题目内容
12.将无色液体A与黑色粉末B混合,能产生一种无色无味的气体C.若将红热的银白色金属D放入C中,剧烈燃烧,火星四射,生成一种黑色固体E,推断并写出上述物质的化学式.AH2O2BMnO2CO2DFeEFe3O4.
分析 根据无色液体A与黑色粉末B混合,立即有大量气体C产生,且C能够支持银白色金属D的燃烧,得知C是氧气,则B为二氧化锰,A液体为过氧化氢溶液;银白色的金属D是铁,生成的黑色固体为四氧化三铁,据此分析.
解答 解:无色液体A与黑色粉末B混合,立即有大量气体C产生,且C能够支持银白色金属D的燃烧,得知C是氧气,则B为二氧化锰,A液体为过氧化氢溶液;银白色的金属D是铁,生成的黑色固体为四氧化三铁,因此:A为过氧化氢,B为二氧化锰,C为氧气,D为铁,E为四氧化三铁,故答案为:H2O2;MnO2;O2;Fe;Fe3O4.
点评 推断习题要善于根据习题中的信息来寻找突破口,抓住解决问题的关键,比如本题中的“气体C能支持燃烧”既是解决此题的关键突破口.当然学生还得有过硬的基础知识根基.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列有关空气中各成分说法正确的是( )
| A. | 氧气化学性质比较活泼,能燃烧 | |
| B. | 氮气的化学性质不活泼,可在食品包装时充入防腐 | |
| C. | 稀有气体不与其他物质发生反应 | |
| D. | 二氧化碳是一种气体污染物 |
20.下列过程能使空气中CO2含量减少的是( )
| A. | 动物呼吸 | B. | 光合作用 | C. | 煤燃烧 | D. | 砍伐树木? |
7.下列说法正确的是( )
| A. | 溶质一定是固体 | B. | 均一、稳定的物质肯定是溶液 | ||
| C. | 溶液一定是无色的 | D. | 溶液一定是混合物 |
17.下列说法错误的是( )
| A. | 水分子是保持水化学性质的最小粒子 | |
| B. | 原子是化学变化中的最小粒子 | |
| C. | 同种元素的原子,质子数一定相同 | |
| D. | 分子可再分,原子不能再分 |
1.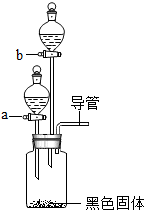 不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.
不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.
探究一:“鱼浮灵”的主要成分是什么?
【查阅资料】过碳酸钠,白色结晶颗粒,易溶于水并迅速放出氧气.
【猜想假设】“鱼浮灵”的主要成分是过碳酸钠.
【设计方案】
【结果分析】主要成分是过碳酸钠.根据化学反应方程式:X+H2O═NaCO3+H2O2,推出过碳酸钠的化学式X为Na2CO4.
【实验反思】
(1)仪器a和b的名称是分液漏斗.
(2)实验①中的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)实验②不严密,应该补充实验生成的气体通入澄清的石灰水.
(4)“鱼浮灵”的保存方法是密封,置阴凉处.
为了储存、运输、使用的方便,工业上采用醇析法将其转化成固态的过碳酸钠晶体.
探究二:工业上使用的过碳酸钠晶体(xNa2CO3.yH2O2)的组成.
【设计实验】称取若干份质量为7.85g过碳酸钠晶体备用.
方案:通过测定碳酸盐沉淀的质量,进而求得碳酸钠的质量.
取一份过碳酸钠晶体溶于水,向所得溶液中滴加过量的CaCl2溶液,过滤、洗涤、烘干,得到白色沉淀,称量.
(1)滴加的CaCl2溶液要过量的原因是将Na2CO3 完全转化为沉淀.
(2)洗涤沉淀的目的是除去表面可溶性杂质CaCl2、NaCl.
(3)检验沉淀已经洗涤干净的方法是取最后一滴洗涤液,滴加AgNO3若无沉淀出现,则表示已经洗净,则表示已经洗净.
【实验结果】实验测得碳酸钙的质量为5g,请通过计算得出过碳酸钠晶体(xNa2CO3.yH2O2)的化学式.
【实验反思】若CaCO3沉淀过滤后不洗涤,则x:y的值将偏大(填“偏大”“偏小”或“无影响”).
 不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.
不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.探究一:“鱼浮灵”的主要成分是什么?
【查阅资料】过碳酸钠,白色结晶颗粒,易溶于水并迅速放出氧气.
【猜想假设】“鱼浮灵”的主要成分是过碳酸钠.
【设计方案】
| 实验 | 主要操作步骤 | 主要实验现象 | 结论 |
| ① | 在集气瓶中加入少量二氧化锰(黑色固体),在仪器a中加入新配制的“鱼浮灵”的饱和水溶液;打开仪器a的活塞,放出适量溶液后,在导管口放一根带火星的木条 | 有气泡逸出,能使带火星木条复燃 | “鱼浮灵”溶于水生成过氧化氢 |
| ② | 关闭仪器a,在仪器b中加入稀盐酸,打开活塞,放出适量溶液后,在导管口放一燃着的木条 | 生成大量无色气泡,木条熄灭 | “鱼浮灵”溶于水生成碳酸钠 |
【实验反思】
(1)仪器a和b的名称是分液漏斗.
(2)实验①中的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)实验②不严密,应该补充实验生成的气体通入澄清的石灰水.
(4)“鱼浮灵”的保存方法是密封,置阴凉处.
为了储存、运输、使用的方便,工业上采用醇析法将其转化成固态的过碳酸钠晶体.
探究二:工业上使用的过碳酸钠晶体(xNa2CO3.yH2O2)的组成.
【设计实验】称取若干份质量为7.85g过碳酸钠晶体备用.
方案:通过测定碳酸盐沉淀的质量,进而求得碳酸钠的质量.
取一份过碳酸钠晶体溶于水,向所得溶液中滴加过量的CaCl2溶液,过滤、洗涤、烘干,得到白色沉淀,称量.
(1)滴加的CaCl2溶液要过量的原因是将Na2CO3 完全转化为沉淀.
(2)洗涤沉淀的目的是除去表面可溶性杂质CaCl2、NaCl.
(3)检验沉淀已经洗涤干净的方法是取最后一滴洗涤液,滴加AgNO3若无沉淀出现,则表示已经洗净,则表示已经洗净.
【实验结果】实验测得碳酸钙的质量为5g,请通过计算得出过碳酸钠晶体(xNa2CO3.yH2O2)的化学式.
【实验反思】若CaCO3沉淀过滤后不洗涤,则x:y的值将偏大(填“偏大”“偏小”或“无影响”).
2. 2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )
2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )
 2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )
2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )| A. | 纳米材料 | B. | 有机合成材料 | C. | 复合材料 | D. | 金属或合金 |