题目内容
已知氢氧化锂(LiOH)可溶于水,其化学性质与氢氧化钠相似。下列对氢氧化锂的化学性质的说法中错误的是( )
A. 能与二氧化碳反应
B. 能使无色酚酞试液变红
C. 能与稀硫酸反应
D. 能使紫色石蕊试液变红
D 【解析】氢氧化锂和氢氧化钠的化学性质相似,能和二氧化碳反应生成盐和水;其溶液呈碱性,能使酚酞溶液变红,能使紫色石蕊溶液变蓝,能和酸发生中和反应,故选D.某研究小组对自动充气气球(示意图如图1)进行下列探究.
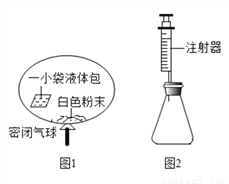
【查阅资料】该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为了检验气体是二氧化碳,可选用____(填试剂名称),反应方程式为_______________。
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈_____性。
探究二:白色粉末成分的探究
【猜想与假设】
甲同学认为是碳酸钙; 乙同学认为是碳酸钠; 丙同学认为是碳酸氢钠。
【设计并进行实验】
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明________同学的猜想不正确。
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
① | 碳酸氢钠 | 5 | V1 |
② | 碳酸钠 | 5 | V2 |
③ | 白色粉末 | x | V1 |
实验①的化学方程式为__________;表中x=_____;V1 ____V2(填“>”、“<”或“=”)。
【分析并得出结论】:
(5)白色粉末是_________。
澄清石灰水 Ca(OH)2 + CO2 = CaCO3↓+ 2H2O 酸 甲 NaHCO3 + HCl = NaCl +H2O +CO2↑ 5 > 碳酸氢钠 【解析】(1)为了检验气体是二氧化碳,可选用澄清石灰水,二氧化碳可使石灰水变浑浊,反应方程式为Ca(OH)2 + CO2 = CaCO3↓+ 2H2O。探究一:液体包内溶液酸碱性的探究。(2)室温时,用pH试纸测得溶液的pH=3,则该溶...化学兴趣小组为验证质量守恒定律,做了镁条在空气中然烧的实验(如图1)。

同学们观察到镁条在空气中剧烈燃烧,发出耀眼的白光,因此镁在军事上作_________;
同时同学们还观察到产生的大量白烟弥漫到空气中,最后一些白色固体掉落在仪器A上。
(1)上述仪器A名称是____________。
(2)同学们通过称量发现:在仪器A上收集到产物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:____________。
(3)小红按下图2装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁( Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
实验操作 | 实验现象及结论 |
_______________________ | ________________ |
【反思与交流】
①写出镁条燃烧生成氮化镁的化学方程式为____________________;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:_________________;
③同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识:___________
照明弹、信号弹、闪光弹、诱饵弹等 石棉网 反应生成的氧化镁部分扩散到空气中 取适量黄色固体样品于试管中,向试管中加入适量水,在试管口放湿润的红色石蕊试纸 湿润的红色石蕊试纸变蓝色,说明黄色固体是氮化镁 3Mg+N22Mg3N2 相同条件下,氧气比氮气更容易和镁反应 燃烧不一定需要氧气 【解析】镁条燃烧生成氧化镁,反应的化学方程式为:2Mg+O22MgO,因此镁在军事上作照明弹、信号弹、闪...
