题目内容
当SO2和SO3的质量比为4:1时,其氧原子个数比为 .
考点:化合物中某元素的质量计算
专题:化学式的计算
分析:根据题意,结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:当SO2和SO3的质量比为4:1时,设它们的质量分别为4m、m,所含氧元素的质量比为(4m×
×100%):(m×
×100%)=10:3;氧元素的质量比即为所含氧原子的个数比,故所含氧原子的个数比是10:3.
故答案为:10:3.
| 16×2 |
| 32+16×2 |
| 16×3 |
| 32+16×3 |
故答案为:10:3.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
下列对质量守恒定律的理解,正确的是( )
| A、因为“质量守恒”,所以煤燃烧后产生的煤渣质量一定和反应前煤的质量相等 |
| B、镁条在空气中燃烧后,生成物的质量比镁的质量大 |
| C、100g水与100g酒精混合后,质量等于200g,这符合质量守恒定律 |
| D、1g氢气在9g氧气中完全燃烧生成了10水 |
分析HCl、X、HClO、KClO3、KClO4的排列顺序规律,可知X代表的是( )
| A、NaCl |
| B、Ca(ClO)2 |
| C、Cl2 |
| D、Cl2O3 |
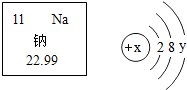 图示元素周期表中的一格和该元素的原子结构示意图,下列叙述不正确的是( )
图示元素周期表中的一格和该元素的原子结构示意图,下列叙述不正确的是( )| A、该元素为金属元素 |
| B、x值为11,y值为1 |
| C、该元素的相对原子质量为22.99 |
| D、该元素的原子失去电子形成离子,其离子符号为Na- |
 为了检验活性炭的性质,某同学做了一个小实验,如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入少量的活性炭,将会出现什么现象?
为了检验活性炭的性质,某同学做了一个小实验,如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入少量的活性炭,将会出现什么现象?