题目内容
下表中填入的是核电荷数从1到18的部分元素的原子结构示意图。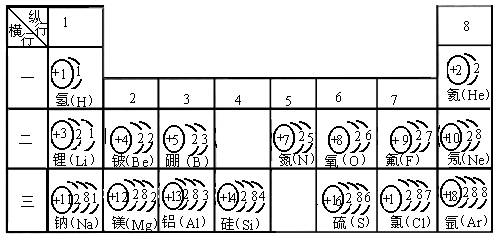
(1)在下列提供的四种元素中,选择相应元素填入上表的空格内(填序号)。
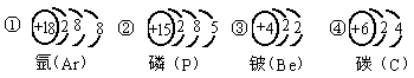
(2)阅读下列短文,回答问题:
实验证明,在上表同一横行中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强;在同一纵行中,从上到下,原子失去电子的能力增强,得到电子的能力减弱。实验还证明,失去电子能力越强的元素,其最高价氧化物的水化物(氢氧化物)的碱性就越强;得到电子能力越强的元素,其最高价氧化物的水化物(含氧酸)的酸性越强,它跟氢气化合形成的氢化物也更稳定。
①在上表元素中,失去电子能力最强的原子是________,得到电子能力最强的原子是________。
②下列判断正确的是________。
A.碱性:Mg(OH)2>Al(OH)3 B.酸性:H2SO4>HClO4(高氯酸)
C.氢化物的稳定性:H2O>H2S D.得到电子能力:Si>N
(3)某元素的原子结构示意图为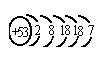 ,则该元素的化学性质跟上表中第________纵行的元素的化学性质最相似。
,则该元素的化学性质跟上表中第________纵行的元素的化学性质最相似。
答案:
解析:
提示:
解析:
| (1)第二横行的空格内填写④;第三横行的空格内填写②
(2)①钠(或Na) 氟(或F);②A、C (3)7
|
提示:
| 在元素周期表中,横行中元素的原子核内质子数依次增大,每个纵行的原子的最外层电子数相等。
|

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
 如表是某品牌矿泉水标签的一部分.
如表是某品牌矿泉水标签的一部分.
(1)表中有________种元素,表中化学符号表示构成物质的三种粒子中的________,另外两种粒子是________、________.
(2)根据原子结构示意图判断,该元素原子的核电荷数为________,核外有________个电子层.在化学反应中这种原子容易________电子,形成________(从上表中选择化学符号填入).
(3)根据下表写出.
| 化学符号 | Ca2+ | Mg2+ | 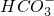 (碳酸氢根) | 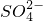 |
| 化合价 | +2 | +2 | -1 | -2 |
(4)化学符号可以表示一定的意义.例如SO42-可以表示________(写出三种).
 如表是某品牌矿泉水标签的一部分.
如表是某品牌矿泉水标签的一部分.



 判断,该元素原子的核电荷数为____________,核外有____________个电子层。在化学反应中这种原子容易____________电子,形成____________(从上表中选择化学符号填入)。
判断,该元素原子的核电荷数为____________,核外有____________个电子层。在化学反应中这种原子容易____________电子,形成____________(从上表中选择化学符号填入)。