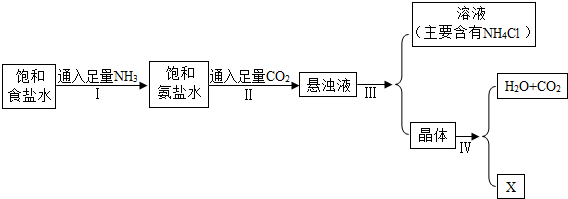
题目内容
工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠,现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应,反应过程中烧杯内物质的质量随时间的变化关系如图所示.求:样品中碳酸钠的质量分数.
【答案】分析:由于碳酸钠和稀盐酸反应能产生二氧化碳,并从烧杯中逸出,因此烧杯中物质变化的质量就是生成二氧化碳的质量.由生成二氧化碳的质量根据碳酸钠与稀盐酸反应的化学方程式可以计算出样品中碳酸钠的质量.进而求出碳酸钠的质量分数.
解答:解:由图象可知,反应中生成CO2的质量为84.8g-80.4g=4.4g
设样品中碳酸纳的质量为x
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 44
x 4.4g
x=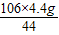 =10.6g
=10.6g
原样品中碳酸纳的质量分数为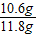 ×100%=89.8%
×100%=89.8%
答:原样品中碳酸纳的质量分数为89.8%.
点评:对变化的曲线进行分析时,曲线的折点往往意味着恰好完全反应,此时总质量与反应前总质量的差即为反应放出气体的质量.
解答:解:由图象可知,反应中生成CO2的质量为84.8g-80.4g=4.4g
设样品中碳酸纳的质量为x
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 44
x 4.4g
x=
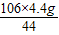 =10.6g
=10.6g 原样品中碳酸纳的质量分数为
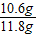 ×100%=89.8%
×100%=89.8%答:原样品中碳酸纳的质量分数为89.8%.
点评:对变化的曲线进行分析时,曲线的折点往往意味着恰好完全反应,此时总质量与反应前总质量的差即为反应放出气体的质量.

练习册系列答案
相关题目