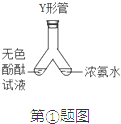
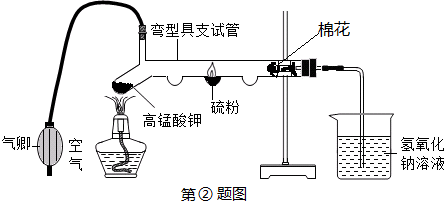
题目内容
同学们用二氧化锰催化过氧化氢溶液的方法制氧气时,探究了影响化学反应速率的部分因素,实验数据如下表:| 实验 序号 | 过氧化氢溶液浓度∕% | 过氧化氢溶液体积∕m L | 温度∕℃ | 二氧化锰的用量∕g | 收集氧气的体积∕m L | 反应所需的时间∕s |
| Ⅰ. | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| Ⅱ. | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| Ⅲ. | 30 | 5 | 35 | 2 | 49.21 | |
| Ⅳ. | 30 | 5 | 55 | 2 | 10.76 |
(2)从实验Ⅲ和Ⅳ对比可知,化学反应速率与温度的关系是______;
(3)学习了双氧水制氧气的实验后,王林同学想起自己家里有一瓶消毒用的双氧水,经查看发现已过期,他用实验证明了这瓶双氧水已经完全变质.请你猜想王林同学的实验操作是:______.
(4)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量是减小、不变还是增大呢?______.
【答案】分析:(1)过氧化氢分解产生氧气和水,可以据此写出该反应的化学方程式;
(2)比较表格中的数据在其他条件都相同时,可以看出过氧化氢的浓度、温度等对化学反应速率的影响;
(3)根据双氧水在二氧化锰催化剂的条件下分解生成氧气的原理解答.
(4)由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变;
解答:解:(1)过氧化氢分解产生了氧气和水,所以可以写出该反应的化学方程式:2H2O2 MnO2.2H2O+O2↑;
(2)从表中分析可知:①②中除了过氧化氢浓度不同之外,其他的各种量均相同,所以可以判断出是反应物的浓度影响了反应速率,并且是浓度越大,反应速率越快;③④则是温度不同其他条件相同,温度高的反应速率快;
(3)取适量该双氧水,加入适量二氧化锰,不产生气泡.说明已变质
(4)根据质量守恒定律可以知道,生成物的质量只与反应物的质量多少有关,而与反应物的浓度无关,所以本题中是向过氧化氢溶液中加入了水,而没有改变过氧化氢溶液中溶质的质量,所以产生氧气的质量不会改变;
故答案为:(1)反应物浓度;
(2)温度越高,化学反应速率越快;
(3)取适量该双氧水,加入适量二氧化锰,不产生气泡.
(4)不变
点评:本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案.
(2)比较表格中的数据在其他条件都相同时,可以看出过氧化氢的浓度、温度等对化学反应速率的影响;
(3)根据双氧水在二氧化锰催化剂的条件下分解生成氧气的原理解答.
(4)由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变;
解答:解:(1)过氧化氢分解产生了氧气和水,所以可以写出该反应的化学方程式:2H2O2 MnO2.2H2O+O2↑;
(2)从表中分析可知:①②中除了过氧化氢浓度不同之外,其他的各种量均相同,所以可以判断出是反应物的浓度影响了反应速率,并且是浓度越大,反应速率越快;③④则是温度不同其他条件相同,温度高的反应速率快;
(3)取适量该双氧水,加入适量二氧化锰,不产生气泡.说明已变质
(4)根据质量守恒定律可以知道,生成物的质量只与反应物的质量多少有关,而与反应物的浓度无关,所以本题中是向过氧化氢溶液中加入了水,而没有改变过氧化氢溶液中溶质的质量,所以产生氧气的质量不会改变;
故答案为:(1)反应物浓度;
(2)温度越高,化学反应速率越快;
(3)取适量该双氧水,加入适量二氧化锰,不产生气泡.
(4)不变
点评:本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
结合图示实验装置,回答下列问题.
(1)写出图中标号仪器的名称① ;② ;③ .
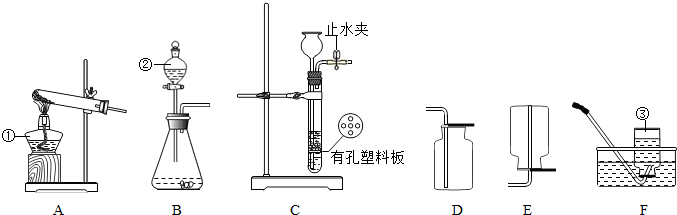
(2)实验室用锌粒和稀硫酸制取氢气的化学方程式为: .
若用C装置制取氢气,检查气密性的方法是 ,要想使该装置能更有效地达到控制反应的发生和停止,应将锌粒放在有孔塑料板的 (填“上面”或“下面”),其原理是 .
(3)实验室常用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气,已知氨气的密度小于空气,易溶于水且能和水反应.则实验室制取氨气的发生装置为 (填字母编号,下同),收集装置为 .
(4)实验室用二氧化锰催化双氧水制取氧气,发生装置为 (从“A、B”中选择),收集装置为 ,反应的化学方程式为: .
(5)某化学兴趣小组同学想探究FeCl3溶液是否对过氧化氢的分解具有催化作用.
①请你帮助他们完成实验报告:
②经分析知:FeCl3溶液中存在H20、Fe3+和Cl-三种微粒,于是同学们提出了以下猜想:
甲同学:催化分解H202的是FeCl3溶液中的H20;
乙同学:催化分解H202的是FeCl3溶液中的Fe3+;
丙同学:催化分解H202的是FeCl3溶液中的Cl-.
你认为最不可能的是 同学的猜想,理由是 .
③同学们对余下的两个猜想,用实验进行了探究.请你仔细分析后填表:
(1)写出图中标号仪器的名称①

(2)实验室用锌粒和稀硫酸制取氢气的化学方程式为:
若用C装置制取氢气,检查气密性的方法是
(3)实验室常用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气,已知氨气的密度小于空气,易溶于水且能和水反应.则实验室制取氨气的发生装置为
(4)实验室用二氧化锰催化双氧水制取氧气,发生装置为
(5)某化学兴趣小组同学想探究FeCl3溶液是否对过氧化氢的分解具有催化作用.
①请你帮助他们完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加5%的H202溶液,然后滴人适量的FeCl3溶液,把带火星的木条伸入试管. | FeCl3溶液可以 催化分解H202 |
甲同学:催化分解H202的是FeCl3溶液中的H20;
乙同学:催化分解H202的是FeCl3溶液中的Fe3+;
丙同学:催化分解H202的是FeCl3溶液中的Cl-.
你认为最不可能的是
③同学们对余下的两个猜想,用实验进行了探究.请你仔细分析后填表:
| 实验过程 | 实验现象 | 结论 |
| 向盛有5%的H202溶液的试管中加入少量的盐酸(含有Cl-),并把带火星的木条伸人试管. | 无明显现象 | |
| 向盛有5%的H202溶液的试管中加入少量的Fe2(S04)3溶液(含有Fe3+),并把带火星的木条伸人试管. |
结合图示实验装置,回答下列问题.
(1)写出图中标号仪器的名称①________;②________;③________.

(2)实验室用锌粒和稀硫酸制取氢气的化学方程式为:________.
若用C装置制取氢气,检查气密性的方法是________,要想使该装置能更有效地达到控制反应的发生和停止,应将锌粒放在有孔塑料板的________(填“上面”或“下面”),其原理是________.
(3)实验室常用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气,已知氨气的密度小于空气,易溶于水且能和水反应.则实验室制取氨气的发生装置为________ (填字母编号,下同),收集装置为________.
(4)实验室用二氧化锰催化双氧水制取氧气,发生装置为________(从“A、B”中选择),收集装置为________,反应的化学方程式为:________.
(5)某化学兴趣小组同学想探究FeCl3溶液是否对过氧化氢的分解具有催化作用.
①请你帮助他们完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加5%的H202溶液,然后滴人适量的FeCl3溶液,把带火星的木条伸入试管. | FeCl3溶液可以 催化分解H202 |
甲同学:催化分解H202的是FeCl3溶液中的H20;
乙同学:催化分解H202的是FeCl3溶液中的Fe3+;
丙同学:催化分解H202的是FeCl3溶液中的Cl-.
你认为最不可能的是________同学的猜想,理由是________.
③同学们对余下的两个猜想,用实验进行了探究.请你仔细分析后填表:
| 实验过程 | 实验现象 | 结论 |
| 向盛有5%的H202溶液的试管中加入少量的盐酸(含有Cl-),并把带火星的木条伸人试管. | 无明显现象 | |
| 向盛有5%的H202溶液的试管中加入少量的Fe2(S04)3溶液(含有Fe3+),并把带火星的木条伸人试管. |