题目内容
(1)将100g质量分数为36.5%的盐酸稀释为质量分数为10%的盐酸,需要加水的质量是多少?
(2)用146g质量分数为10%的盐酸与25g大理石恰好完全反应(大理石中的杂质不参加反应).计算该大理石中碳酸钙的质量分数.
(2)用146g质量分数为10%的盐酸与25g大理石恰好完全反应(大理石中的杂质不参加反应).计算该大理石中碳酸钙的质量分数.
考点:根据化学反应方程式的计算,用水稀释改变浓度的方法
专题:溶液的组成及溶质质量分数的计算,有关化学方程式的计算
分析:(1)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
(2)由146g质量分数为10%的盐酸的质量,由碳酸钙与盐酸反应的化学方程式,计算出25g大理石中碳酸钙的质量,进而计算该大理石中碳酸钙的质量分数即可.
(2)由146g质量分数为10%的盐酸的质量,由碳酸钙与盐酸反应的化学方程式,计算出25g大理石中碳酸钙的质量,进而计算该大理石中碳酸钙的质量分数即可.
解答:解:(1)设要加水的质量为x,根据溶液稀释前后,溶质的质量不变,
则100g×36.5%=(100g+x)×10% x=265g.
(2)设该大理石中碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
y 146g×10%
=
y=20g
该大理石中碳酸钙的质量分数为
×100%=80%.
答:(1)需要加水的质量是265g;(2)该大理石中碳酸钙的质量分数为80%.
则100g×36.5%=(100g+x)×10% x=265g.
(2)设该大理石中碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
y 146g×10%
| 100 |
| 73 |
| y |
| 146g×10% |
该大理石中碳酸钙的质量分数为
| 20g |
| 25g |
答:(1)需要加水的质量是265g;(2)该大理石中碳酸钙的质量分数为80%.
点评:本题难度不大,掌握化学方程式的有关计算、溶液稀释前后溶质的质量不变是正确解答本题的关键所在.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学是在分子、原子层次上研究物质的:①性质 ②组成 ③结构 ④变化规律的科学.你认为其中正确的是( )
| A、①②③ | B、③④ |
| C、①②④ | D、全部 |
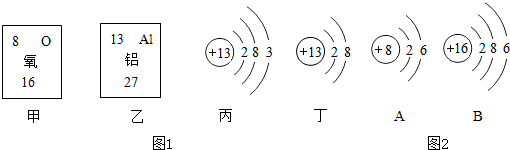
 甲、乙、丙分别是硫磺、红磷、细铁丝在氧气中燃烧的三个实验示意图,请依据示意图和有关的知识回答下列问题:
甲、乙、丙分别是硫磺、红磷、细铁丝在氧气中燃烧的三个实验示意图,请依据示意图和有关的知识回答下列问题: 儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分.
儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分.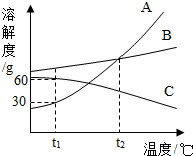 根据如图溶解度曲线回答下列问题:
根据如图溶解度曲线回答下列问题: