题目内容
18.请根据如图所示的实验室中实验装置图填空.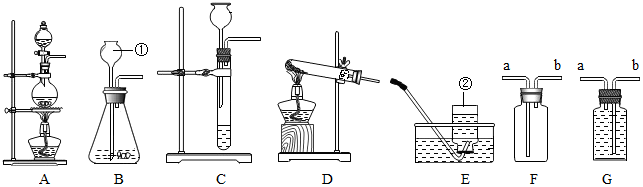
(1)完成图中标有数字的仪器的名称:①长颈漏斗②集气瓶
(2)用高锰酸钾制备氧气时,应选用装置D做气体发生装置(填序号,下同),写出该反应化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室制得的CO2气体中常含有水蒸气.为了得到纯净、干燥的CO2气体,可选用的干燥剂是B(填选项:A.氢氧化钠固体 B.浓硫酸).
(4)有一名同学欲用F装置收集H2,则H2应从导管口b通入;若用G来收集一瓶O2,则O2应从导管口a通入.
(5)已知MnO2固体和浓盐酸混合共热可制得氯气(Cl2),则应选用A做气体发生装置.
分析 (1)熟记仪器的名称;
(2)根据反应物的状态和反应条件选择发生装置,并写出相应的方程式;
(3)根据二氧化碳的性质来分析;
(4)氢气密度比空气小,所以应从短管进气,将空气挤压到集气瓶底部排出;氧气密度比水小,所以应从短管进气,长管便于排水;
(5)根据反应物的状态和反应条件选择发生装置.
解答 解:(1)仪器①是长颈漏斗,②是集气瓶;故填:长颈漏斗;集气瓶;
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,故可选用的气体发生装置是D;反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;故填:D;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)二氧化碳能与氢氧化钠反应,所以不能用氢氧化钠固体来干燥二氧化碳;浓硫酸具有吸水性,所以可用浓硫酸来干燥二氧化碳;故填:B;
(4)氢气密度比空气小,所以应从短管进气,将空气挤压到集气瓶底部排出;氧气密度比水小,所以应从短管进气,长管便于排水;故填:b;a;
(5)MnO2固体和浓盐酸混合共热可制得氯气(Cl2),属于固体和液体反应且须加热,所以选择A装置;故填:A.
点评 明确常用仪器、制取气体的反应原理、装置选取是解答此题的关键,发生装置据反应物状态和反应条件选择,收集装置据气体密度和溶解性选择.

练习册系列答案
相关题目
18.某化学兴趣小组的同学按照课本的实验装置做“测定空气中氧气的体积分数”实验(图1),但测出的氧气体积分数明显小于$\frac{1}{5}$.请你参与探究:
【提出问题】造成误差的原因是什么?如何改进课本实验装置?
【查阅资料】(1)着火点是指可燃物燃烧所需要的最低温度.
(2)白磷和红磷的组成元素、燃烧现象和产物均相同.
(3)铜在空气中加热,和氧气反应生成黑色的氧化铜.

【猜想与假设】
甲同学:可能是导管内原存有空气,后来留有吸入的水,影响实验的准确性;
乙同学:可能是瓶内残留气体中还有氧气的缘故;
你还能做的猜想是红磷不足等
【交流与讨论】
(1)丙同学认为,用木炭代替红磷,就可以消除这个现象,大家认为丙同学的猜想不合理,理由是木炭可以和氧气反应生成二氧化碳气体,不能产生压强差;
(2)他们对课本实验装置进行了如图2的改进(其他仪器忽略).
①甲同学提出应把红磷更换为白磷,理由是白磷的着火点低,可以较容易的发生燃烧,
白磷燃烧的符号表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②通过粗铜丝来点燃玻璃管内的白磷,利用了金属铜的物理性质是导电性;
③与课本实验装置相比,该装置的一个优点是环保,生成的五氧化二磷有毒,不污染空气;测量所得数据比较准确;所用试剂量少,节约药品等.
【探究与反思】
(1)为验证乙同学的猜想,将铜粉在残余气体中加热,观察到铜粉变黑,所以乙同学的猜想合理(选填“合理”或“不合理”).
(2)大家采用改进的实验装置(图2)进行实验,待玻璃管冷却、管内白色的烟幕消失,左管液面上升了1格,得到了较准确的数据,但又意外发现左玻璃管内壁上端附着黄色固体.黄色固体主要成分可能是白磷.
【提出问题】造成误差的原因是什么?如何改进课本实验装置?
【查阅资料】(1)着火点是指可燃物燃烧所需要的最低温度.
(2)白磷和红磷的组成元素、燃烧现象和产物均相同.
(3)铜在空气中加热,和氧气反应生成黑色的氧化铜.
| 颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/g•cm-3 | |
| 红磷 | 暗红色固体 | 590 | 240 | 2.34 |
| 白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |

【猜想与假设】
甲同学:可能是导管内原存有空气,后来留有吸入的水,影响实验的准确性;
乙同学:可能是瓶内残留气体中还有氧气的缘故;
你还能做的猜想是红磷不足等
【交流与讨论】
(1)丙同学认为,用木炭代替红磷,就可以消除这个现象,大家认为丙同学的猜想不合理,理由是木炭可以和氧气反应生成二氧化碳气体,不能产生压强差;
(2)他们对课本实验装置进行了如图2的改进(其他仪器忽略).
①甲同学提出应把红磷更换为白磷,理由是白磷的着火点低,可以较容易的发生燃烧,
白磷燃烧的符号表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②通过粗铜丝来点燃玻璃管内的白磷,利用了金属铜的物理性质是导电性;
③与课本实验装置相比,该装置的一个优点是环保,生成的五氧化二磷有毒,不污染空气;测量所得数据比较准确;所用试剂量少,节约药品等.
【探究与反思】
(1)为验证乙同学的猜想,将铜粉在残余气体中加热,观察到铜粉变黑,所以乙同学的猜想合理(选填“合理”或“不合理”).
(2)大家采用改进的实验装置(图2)进行实验,待玻璃管冷却、管内白色的烟幕消失,左管液面上升了1格,得到了较准确的数据,但又意外发现左玻璃管内壁上端附着黄色固体.黄色固体主要成分可能是白磷.
19.科学实验中,准确地分析实验数据是得到正确科学结论的保证,下列4个图象,能正确反映对应关系的是( )
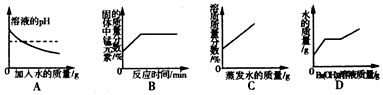

| A. | 常温下,稀释KOH溶液 | |
| B. | 加热一定质量高锰酸钾固体 | |
| C. | 在恒温的条件下,将适量的氯化钠饱和溶液蒸发适量的水分 | |
| D. | 在装有稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量 |
13.已知某粗盐样品中含有Na2SO4、MgCl2、CaCl2等杂质.实验室提纯流程如图:
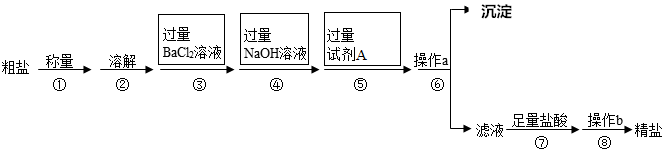
下列说法中不正确的是( )

下列说法中不正确的是( )
| A. | 步骤⑤中的试剂A是碳酸钠溶液 | |
| B. | 通过a操作得到的沉淀中有三种物质 | |
| C. | 操作a和操作b中都用到了玻璃棒,但其操作是不同的 | |
| D. | 加入足量盐酸的目的是除去步骤④、⑤中过量的试剂 |
3.质量守恒定律是帮助我们学习和认识化学反应实质的重要理论.
(1)下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB══cC+dD中一定有:a+b=c+d
(2)有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物后的质量如表,
则x=88;已知参加反应的物质R与氧气的分子个数之比为1:3.则R的相对分子质量是46.
(1)下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB══cC+dD中一定有:a+b=c+d
(2)有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物后的质量如表,
| R | O2 | CO2 | H2O | |
| 反应前质量/g | 46 | 128 | 0 | 0 |
| 反应后质量/g | 0 | 32 | x | 54 |
10.下列各图中能说明分子间的间隔变小的是( )
| A. |  炒菜闻到香味 | B. |  湿衣服晾干 | ||
| C. |  酚酞遇氨水变红 | D. |  压缩空气 |
7.下列各组物质中,前者属于混合物、后者属于单质的是( )
| A. | 蒸馏水 氮气 | B. | 二氧化碳 氢气 | C. | 大理石 空气 | D. | 石油 氧气 |
