题目内容
26、碳酸钠和碳酸氢钠是面食加工常用的物质,一定条件下在面团中能产生二氧化碳气体,经过加热后二氧化碳体积膨胀,在面团中留下许多小孔,使蛋糕等面食制品在食用时松软可口,已知碳酸钠加热不能分解,而碳酸氢钠在加热时能发生分解生成碳酸钠、水、二氧化碳.试回答:
(1)在面团没有发酵的情况下,要使面团松软可口应选择
(2)分别写出碳酸钠和碳酸氢钠与盐酸反应的方程式:
(3)根据上述两个反应分析:要使发酵过的面团 (含有机酸) 更松软最好加
(1)在面团没有发酵的情况下,要使面团松软可口应选择
NaHCO3
(选填“Na2CO3”或“NaHCO3”).(2)分别写出碳酸钠和碳酸氢钠与盐酸反应的方程式:
Na2CO3+2HCl═2NaCl+H2O+CO2↑
、NaHCO3+HCl═NaCl+H2O+CO2↑
.(3)根据上述两个反应分析:要使发酵过的面团 (含有机酸) 更松软最好加
NaHCO3
(选填“Na2CO3”或“NaHCO3”),简述这样做的理由等量的酸与NaHCO3产生的二氧化碳多
.分析:(1)没有发酵时面团中不含有酸,碳酸钠不能与酸发生且加热时不能分解,因此无法产生气体二氧化碳,而碳酸氢钠却可以在未与酸反应时受热分解出二氧化碳;
(2)根据含有碳酸根离子的物质能与盐酸反应放出二氧化碳的反应规律,结合碳酸钠、碳酸氢钠的化学性质,写出两物质与盐酸反应的化学方程式;
(3)要使发酵过的面团 (含有机酸) 更松软则需要产生更多的气体二氧化碳,对比两种物质分别与盐酸反应的化学方程式,面团发酵产生的酸与碳酸氢钠反应放出气体二氧化碳的量是碳酸钠的两倍.
(2)根据含有碳酸根离子的物质能与盐酸反应放出二氧化碳的反应规律,结合碳酸钠、碳酸氢钠的化学性质,写出两物质与盐酸反应的化学方程式;
(3)要使发酵过的面团 (含有机酸) 更松软则需要产生更多的气体二氧化碳,对比两种物质分别与盐酸反应的化学方程式,面团发酵产生的酸与碳酸氢钠反应放出气体二氧化碳的量是碳酸钠的两倍.
解答:解:(1)碳酸钠只能遇到酸才能放出二氧化碳气体,而碳酸氢钠在受热时也可分解放出二氧化碳气体,因此在面团没有发酵而没有酸的情况下,在面团中加入受热即可放出二氧化碳的碳酸氢钠,可使面食松软可口;
(2)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑;碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑;
(3)根据碳酸钠和碳酸氢钠与盐酸反应的方程式,在消耗同样的酸时,与碳酸氢钠反应放出二氧化碳是与碳酸钠反应放出二氧化碳的两倍,因此,使用碳酸氢钠时会产生更多的气体二氧化碳而使食品更松软.
故答案为:
(1)NaHCO3;
(2)Na2CO3+2HCl═2NaCl+H2O+CO2↑;NaHCO3+HCl═NaCl+H2O+CO2↑;
(3)NaHCO3;等量的酸与NaHCO3产生的二氧化碳多.
(2)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑;碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑;
(3)根据碳酸钠和碳酸氢钠与盐酸反应的方程式,在消耗同样的酸时,与碳酸氢钠反应放出二氧化碳是与碳酸钠反应放出二氧化碳的两倍,因此,使用碳酸氢钠时会产生更多的气体二氧化碳而使食品更松软.
故答案为:
(1)NaHCO3;
(2)Na2CO3+2HCl═2NaCl+H2O+CO2↑;NaHCO3+HCl═NaCl+H2O+CO2↑;
(3)NaHCO3;等量的酸与NaHCO3产生的二氧化碳多.
点评:本题以生活情境为平台考查碳酸钠与碳酸氢钠性质的异同,利用化学知识解释生活现象,很好在体现出化学对生活的指导作用.

练习册系列答案
相关题目
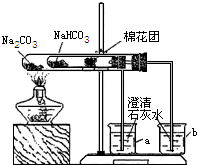 某校同学对市场上的食品疏松剂进行了如下探究.
某校同学对市场上的食品疏松剂进行了如下探究.实验一:甲小组的同学收集到一包主要成分是小苏打(碳酸氢钠)的疏松剂
(1)取样品溶于适量的水中,测得溶液的pH大于7.
(2)向小苏打样品中滴加盐酸,有大量气泡产生,经检验该气体是二氧化碳.该反应的化学方程式为
(3)同学们通过查阅资料,在老师的指导下采用了如图所示装置用小苏打和纯碱做了对比实验.实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,
b烧杯中石灰水了现白色浑浊.试回答:①在实验结束时,操作上要注意的问题是:
②由实验(3)可以得出的结论是
实验二:乙小组的同学收集到一包名为“臭粉”的疏松剂,为探究其组成,进行实验:
(1)“臭粉”为一种白色固体,易溶于水;
(2)取少量样品与稀盐酸混合后产生了可以使石灰水变混浊的气体;
(3)取少量样品加热后,产生了有刺激性气味的气体;
(4)少量样品与氢氧化钠溶液混合后共热,产生了使湿润的红色石蕊试纸变蓝的臭气.
调查后得知,“臭粉”的主要成分是初中化学课本中一种常见的盐.
①你认为该盐是
②用“臭粉”作疏松剂的油炸食品放置后再销售和食用的原因可能是
③某些小商贩喜欢选用“臭粉”代替“小苏打”作疏松剂的原因可能是
实验三:丙小组同学探究小苏打、“臭粉”在制作食品过程中产生气泡的原因
(1)两种疏松剂产生的气体中都含有
(2)小组的同学将少许面粉加入水中取上层液体用pH试纸测得:pH=7.猜测产生气体的原因是
实验四:丁小组的同学在某超市发现一种复合疏松剂--发酵粉,其成分见表:
| 成分 | 所用物质 |
| 碳酸盐类 | 碳酸氢钠 |
| 酸性物质 | 柠檬酸、酒石酸等 |
| 疏松剂 | 明矾 |
| 其他成分 | 淀粉、脂肪酸等 |
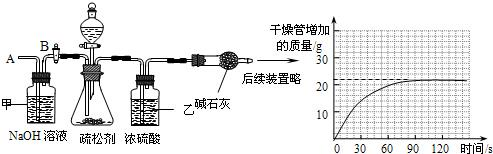
(2)为测定其中碳酸氢钠的质量分数,小组的同学设计了如下实验,其主要实验步骤如下:
Ⅰ.按图组装仪器,将50.0g试样放入锥形瓶中,加入足量某酸溶液;
Ⅱ.测量一定时间内干燥管内物质增加的质量(见下列曲线);
Ⅲ.待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
Ⅳ.再次称量干燥管内物质增加的质量;
Ⅴ.重复Ⅲ和Ⅳ的操作,直至干燥管内物质质量不变.
讨论:
①步骤Ⅰ.加入样品前还应检查
②装置乙的作用是
③请利用有关数据计算试样中碳酸氢钠的质量分数.(写出计算过程,本小题4分)
 17、17、研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
17、17、研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
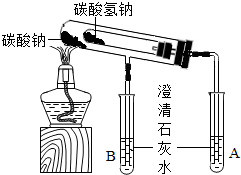
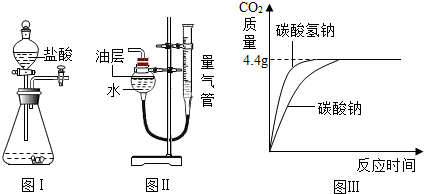
 (2012?河西区二模)校兴趣小组对碳酸钠和碳酸氢钠的性质进行进研究,请你参与并完成相关问题.
(2012?河西区二模)校兴趣小组对碳酸钠和碳酸氢钠的性质进行进研究,请你参与并完成相关问题.