题目内容
19.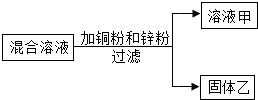 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:(1)若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Cu(NO3)2和Zn(NO3)2;
(2)若向固体乙上滴加盐酸有气泡产生,则固体乙中一定含有Ag、Cu和Zn;
(3)写出一个图中所发生的化学方程式Zn+2AgNO3═2Ag+Zn(NO3)2.
分析 在金属活动性顺序中:Al>Zn>Cu>Ag,根据排在前面的金属可以把位于它后面的金属从其盐溶液中置换出来,可简记为“前置后,盐可溶”,结合实验的现象分析.
解答 解:金属活动性Al>Zn>Cu>Ag,所以锌粉优先与AgNO3发生反应,铜粉后与AgNO3发生反应,但是铜粉和锌粉都不能和Al(NO3)3发生反应,Al(NO3)3一定在溶液中;(1)若溶液甲是蓝色,说明铜已经与AgNO3发生反应,而锌已经全部反应,溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2;
(2)向固体乙上滴加盐酸有气泡产生,说明固体中有锌,锌过量,铜未参加反应,溶液中AgNO3被反应完全,固体中一定含有Ag、Cu和Zn;
(3)锌粉优先与AgNO3发生反应生成硝酸锌和银,因此一定反应,反应的方程式为:Zn+2AgNO3═2Ag+Zn(NO3)2;
故选项为:(1)Al(NO3)3、Cu(NO3)2 和Zn(NO3)2;(2)Ag、Cu和Zn;(3)Zn+2AgNO3═2Ag+Zn(NO3)2.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行分析,活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
9.化学与人类生活的关系非常密切,下列说法你认为正确的是( )
| A. | 燃烧法可以鉴别羊毛和蚕丝 | |
| B. | 钢铁腐蚀、汽油燃烧均属于缓慢氧化 | |
| C. | 加碘食盐可以检验面包中含有淀粉 | |
| D. | 铵态氮肥和熟石灰不能混合使用 |
7.氯化亚铜(CuCl)难溶于水,在空气中迅速被氧化为Cu2(OH)3Cl.以粗盐水(含CaCl2、MgCl2、Na2SO4)、Cu等原料制CuCl的工艺如图.下列说法正确的是( )
(已知:2Cu+2H2SO4+O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O).

(已知:2Cu+2H2SO4+O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O).

| A. | 溶液①②③依次加入,则A为Na2CO3、B为BaCl2 | |
| B. | HCl+NaOH═NaCl+H2O是“反应Ⅱ”中唯一的反应 | |
| C. | 沉淀池中H2O也参与反应且有两种元素的化合价发生变化 | |
| D. | 若CuCl被氧化的原理为:4CuCl+4H2O+O2═2Cu2(OH)3Cl+2A,则A为HCl |
14.下列保存物质的方法及其原因不正确的是( )
| A. | 浓盐酸--防止挥发 | B. | 氢氧化钠--防止潮解和变质 | ||
| C. | 浓硫酸--防止吸水 | D. | 碱石灰--防止氧化 |
11.下列说法不正确的是( )
| A. | 用肥皂水可以区分软水和硬水 | B. | 工业废水不能直接排放 | ||
| C. | 淡水资源是取之不尽用之不竭的 | D. | 过量使用农药化肥会造成水体污染 |
8.如图是某个化学反应前、后的微观模拟图.下面有关图的说法中,正确的是( )

| A. | 该反应的基本类型为化合反应 | |
| B. | 该反应中的生成物属于氧化物 | |
| C. | 反应前后分子的数目保持不变 | |
| D. | 该化学反应中,参加反应的 、 、 和 和 与反应后生成的各粒子间的个数比为1:5:1 与反应后生成的各粒子间的个数比为1:5:1 |