题目内容
【题目】下列实验设计方案不能够达到目的是( )
|
|
|
|
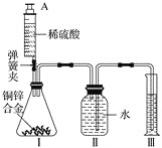
A探究分子运动 | B.探究水的组成 | C探究铁生锈条件 | D.探究影响物质溶解性的因素 |
A. AB. BC. CD. D
【答案】C
【解析】
A、根据大烧杯内小烧杯中的酚酞溶液变红色,进行分析判断。
B、根据电解水的实验结论,进行分析判断。
C、根据铁锈蚀的条件,进行分析判断。
D、要注意变量的控制,注意要除探究要素不同之外,其它条件都应该是相同的。
A、一段时间后,大烧杯内小烧杯中的酚酞溶液变红色,而两者没有直接接触,说明氨分子运动到了酚酞溶液中,选项实验设计方案能够达到目的,不符合题意;
B、电解水生成氢气和氧气,氢气和氧气分别是由氢元素和氧元素组成的,说明水是由氢元素和氧元素组成的,故选项实验设计方案能够达到目的,不符合题意;
C、一段时间后,两支试管中的铁钉均不生锈,不能探究铁生锈条件,故选项实验设计方案不能达到目的,符合题意;
D、图中实验,根据硝酸钾在水和酒精中的溶解情况,可以探究影响物质溶解性的因素之一是溶剂的种类,故选项实验设计方案能够达到目的,不符合题意。故选C。

【题目】把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
物质 | A | B | C | D |
反应前质量 |
|
|
|
|
反应后质量 | 待测 |
| 0 |
|
下列说法正确的是![]()
A. 物质C一定是反应物,物质D可能是单质
B. 反应后密闭容器中A的质量为![]()
C. 反应过程中,物质B和物质D变化的质量比为87:36
D. 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1
【题目】2009年邵阳市九年级化学实验操作技能考试中,小聪同学抽到的试题是“探究酸和碱之间的中和反应“。他向盛有氢氧化钠溶液的烧杯中缓慢滴加稀盐酸,一会儿后,想起忘记加指示剂了,便补加几滴无色酚酞溶液,搅拌,观察到溶液不变色,于是他得出“酸碱恰好完全中和”的结论。
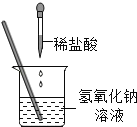
(1)该中和反应的化学方程式是_____;
(2)老师给予小聪的评定是结论不准确。请你帮小聪分析老师的理由是:_____
(3)请你另外设计一个实验,探究小聪实验后烧杯中的溶液是否“恰好完全中和”。
填写下表:
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | _____ |
_____ | _____ |
【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),化学小组的同学询问老师后知道是NaCl、NaOH、Na2CO3、NaHCO3中的某一种溶液。为确认原瓶中是何种溶质的溶液并判断其是否变质化学小组的同学进行了如下的探究活动:

(做出猜想)
猜想a:原溶液的溶质是NaCl 猜想b:原溶液的溶质是NaOH
猜想c:原溶液的溶质是Na2CO3 猜想d:原溶液的溶质是 NaHCO3
(查阅资料)
常温下,有关物质的相关信息如表
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知原溶液的溶质一定不是NaHCO3,因为_____。
(进行实验)
(1)取少量样品测得溶液的pH大于7,则原溶液的溶质肯定不是_____。
(2)下列检测溶液pH的实验操作方法中,正确的是_____(填字母序号)。
A 将pH试纸直接插入待测液中
B 将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸
C 将pH试纸湿润后放在表面皿上,用千净的玻璃棒蘸取待测液滴在pH试纸上
D 读数时将pH试纸呈现的颜色与标准比色卡对照
(3)同学们另取样品又进行了如下实验,实验过程如图:

①生成白色沉淀A的化学反应方程式_____。
②通过实验可以判断样品无色溶液中含有的溶质是_____和_____(填化学式)
(得出结论)
实验完成后,最终得到的结论:原瓶溶液中的溶质是_____,且已变质。