题目内容
实验室有如图所示的实验装置:
结合装置回答有关问题:
①写出图中有标号仪器的名称:m.______.
②实验室可以通过多种途径制得氧气.实验室若用氯酸钾和二氧化锰的混合物制取氧气,应选择发生装置为______(填字母序号),化学方程式为______△2KCl+3O2↑
【答案】分析:①依据常用仪器回答;
②依据氯酸钾制取氧气的反应物的状态和反应条件及反应原理分析解答;
③依据收集气体的装置特点回答;
④根据方程式可知,生成1mol 二氧化碳,需要1mol的碳酸钙,由此可知碳酸钙的物质的量;并据二氧化碳的物质的量和方程式可求出参加反应的盐酸溶质的量,并求出其溶质的质量分数.
解答:解:①标号仪器是长颈漏斗;
②用氯酸钾和二氧化锰的混合物制取氧气,需要加热,故选发生装置A;氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,方程式是:2KClO3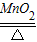 2KCl+
2KCl+
3O2↑;
③装置C收集二氧化碳的方法叫向上排空气法;
④根据方程式可知,生成1mol 二氧化碳,需要1mol的碳酸钙,由此可知碳酸钙的物质的量是0.2mol;
设盐酸的物质的量x
CaCO3+2HCl═CaCl2+H2O+CO2↑
2 1
x 0.2mol
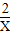 =
=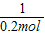
x=0.4mol
稀盐酸的溶质质量分数═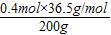 ×100%=7.3%
×100%=7.3%
答:稀盐酸的溶质质量分数7.3%;
故答案为:
①长颈漏斗; ②A; 2KClO3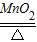 2KCl+3O2↑; ③向上排空气法
2KCl+3O2↑; ③向上排空气法
④0.2; 7.3%.
点评:本题考查了实验室制取二氧化碳的收集方法、氯酸钾制取氧气的反应原理、装置选取,同时考查了学生依据方程式计算的能力,掌握相关知识才能正确分析和解答.
②依据氯酸钾制取氧气的反应物的状态和反应条件及反应原理分析解答;
③依据收集气体的装置特点回答;
④根据方程式可知,生成1mol 二氧化碳,需要1mol的碳酸钙,由此可知碳酸钙的物质的量;并据二氧化碳的物质的量和方程式可求出参加反应的盐酸溶质的量,并求出其溶质的质量分数.
解答:解:①标号仪器是长颈漏斗;
②用氯酸钾和二氧化锰的混合物制取氧气,需要加热,故选发生装置A;氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,方程式是:2KClO3
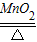 2KCl+
2KCl+3O2↑;
③装置C收集二氧化碳的方法叫向上排空气法;
④根据方程式可知,生成1mol 二氧化碳,需要1mol的碳酸钙,由此可知碳酸钙的物质的量是0.2mol;
设盐酸的物质的量x
CaCO3+2HCl═CaCl2+H2O+CO2↑
2 1
x 0.2mol
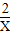 =
=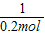
x=0.4mol
稀盐酸的溶质质量分数═
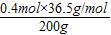 ×100%=7.3%
×100%=7.3%答:稀盐酸的溶质质量分数7.3%;
故答案为:
①长颈漏斗; ②A; 2KClO3
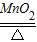 2KCl+3O2↑; ③向上排空气法
2KCl+3O2↑; ③向上排空气法④0.2; 7.3%.
点评:本题考查了实验室制取二氧化碳的收集方法、氯酸钾制取氧气的反应原理、装置选取,同时考查了学生依据方程式计算的能力,掌握相关知识才能正确分析和解答.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
