题目内容
 如图所示,一学生用高锰酸钾制取氧气:
如图所示,一学生用高锰酸钾制取氧气:
(1)指出装置中的错误______;由此可能造成的后果是______;
(2)做此实验的操作第一步是______;
(3)该同学在用此收集方法结束后,发现水开始从导管倒流,这是因为该同学______,此时他可以采取______的措施来补救.
解:(1)试管口少了一团棉花,会使高锰酸钾的小颗粒随气流进入水槽,而使水变成紫红色;
故答案为:没有塞棉花;高锰酸钾进入水中使水槽中的水变成紫红色;
(2)在使用该装置进行气体制取前,应检查装置的气密性,防止因装置漏气而收集不到气体;
故答案为:检查气密性;
(3)导管内出现水倒流应是由于导管没先从水槽中撤出就停止了加热,致使试管内压强减小而引起水倒流;此时可再用酒精灯加热试管或把试管和导管分离,以防止水倒流入试管而引起试管炸裂;
故答案为:先移开酒精灯停止加热,再把导气管从水槽中取出;继续用酒精灯加热试管.
分析:在加热分解高锰酸钾制取氧气时,为防止高锰酸钾的颗粒随气体流入水槽,应在试管口放置一团棉花过滤气体;在进行实验时,应先检查装置的气密性,防止因装置漏气而导致无法收集到气体;实验结束时,应先把导管从水槽中撤出然后再熄灭酒精灯,防止水倒流入试管而使试管遇冷引起试管炸裂.
点评:加热分解高锰酸钾制取氧气的操作为:连接装置--检查装置气密性--加入药品--加热--收集气体--撤导管--熄灭酒精灯.
故答案为:没有塞棉花;高锰酸钾进入水中使水槽中的水变成紫红色;
(2)在使用该装置进行气体制取前,应检查装置的气密性,防止因装置漏气而收集不到气体;
故答案为:检查气密性;
(3)导管内出现水倒流应是由于导管没先从水槽中撤出就停止了加热,致使试管内压强减小而引起水倒流;此时可再用酒精灯加热试管或把试管和导管分离,以防止水倒流入试管而引起试管炸裂;
故答案为:先移开酒精灯停止加热,再把导气管从水槽中取出;继续用酒精灯加热试管.
分析:在加热分解高锰酸钾制取氧气时,为防止高锰酸钾的颗粒随气体流入水槽,应在试管口放置一团棉花过滤气体;在进行实验时,应先检查装置的气密性,防止因装置漏气而导致无法收集到气体;实验结束时,应先把导管从水槽中撤出然后再熄灭酒精灯,防止水倒流入试管而使试管遇冷引起试管炸裂.
点评:加热分解高锰酸钾制取氧气的操作为:连接装置--检查装置气密性--加入药品--加热--收集气体--撤导管--熄灭酒精灯.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
 ,根据你的理解,写出丁烷的一个物理性质
,根据你的理解,写出丁烷的一个物理性质 这是一名初三学生用排水法收集好的一瓶无色气体,则集气瓶中的气体可能是
这是一名初三学生用排水法收集好的一瓶无色气体,则集气瓶中的气体可能是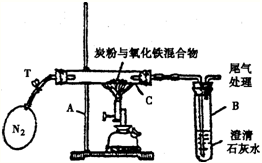 (2005?湘潭)某化学兴趣小组的学生研究过量的碳粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:
(2005?湘潭)某化学兴趣小组的学生研究过量的碳粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下: 如图所示是某学生设计的过滤操作装置图,并用装置将浑浊的河水进行过滤.
如图所示是某学生设计的过滤操作装置图,并用装置将浑浊的河水进行过滤. ,根据你的理解,写出丁烷的一个物理性质______.
,根据你的理解,写出丁烷的一个物理性质______. 这是一名初三学生用排水法收集好的一瓶无色气体,则集气瓶中的气体可能是______(填化学式),请写出实验室制取该气体的化学方程式______.
这是一名初三学生用排水法收集好的一瓶无色气体,则集气瓶中的气体可能是______(填化学式),请写出实验室制取该气体的化学方程式______.
