题目内容
人类生活和工业农业生产都离不开水.下图是自来水厂净水过程的示意图.请根据图示回答问题:(1)自然界的水大多较浑浊说明其中含有______性杂质;
(2)自来水厂使用的净水方法有(填编号)______;
A.沉淀;B.过滤; C.煮沸;D.蒸馏;E.吸附
(3)取水后加入絮凝剂的作用是:______;
(4)活性炭的作用是______;
(5)自来水厂常用二氧化氯进行消毒,二氧化氯的化学式是______.
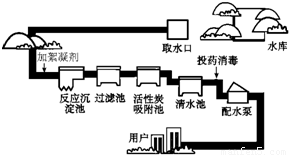
【答案】分析:由图示可知:自来水厂使用的净水方法有沉淀、过滤、吸附;絮凝剂可吸附杂质,使杂质沉降;活性炭具有吸附性;并依据化合物的读法判断化学式.
解答:解:(1)天然水常呈浑浊,因为水中含有许多不溶性杂质;
故答案为:不溶;
(2)由图示可知:自来水厂使用的净水方法有沉淀、过滤、吸附;
故选ABE;
(3)取水后加入絮凝剂可吸附杂质,使杂质沉降;
故答案为:吸附杂质,使杂质沉降;
(4)活性炭具有吸附作用,能除去水中色素和异味等杂质;
故答案为:吸附色素、异味等;
(5)两种元素组成的化合物从后向前可读作“某化某”,所以二氧化氯的化学式是ClO2;
故答案为:ClO2.
点评:本题主要考查了水的净化的相关知识,了解净化水的常用方法、明矾、活性炭的作用是解答此类题的关键.
解答:解:(1)天然水常呈浑浊,因为水中含有许多不溶性杂质;
故答案为:不溶;
(2)由图示可知:自来水厂使用的净水方法有沉淀、过滤、吸附;
故选ABE;
(3)取水后加入絮凝剂可吸附杂质,使杂质沉降;
故答案为:吸附杂质,使杂质沉降;
(4)活性炭具有吸附作用,能除去水中色素和异味等杂质;
故答案为:吸附色素、异味等;
(5)两种元素组成的化合物从后向前可读作“某化某”,所以二氧化氯的化学式是ClO2;
故答案为:ClO2.
点评:本题主要考查了水的净化的相关知识,了解净化水的常用方法、明矾、活性炭的作用是解答此类题的关键.

练习册系列答案
相关题目
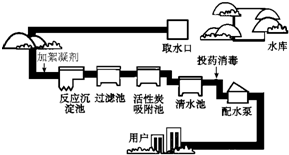 人类生活和工业农业生产都离不开水.下图是自来水厂净水过程的示意图.请根据图示回答问题:
人类生活和工业农业生产都离不开水.下图是自来水厂净水过程的示意图.请根据图示回答问题: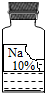 (2013?鹤壁二模)实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
(2013?鹤壁二模)实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
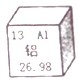 金属盒金属化合物是重要的资源,生活、工业、农业生产都离不开金属盒金属化合物.
金属盒金属化合物是重要的资源,生活、工业、农业生产都离不开金属盒金属化合物.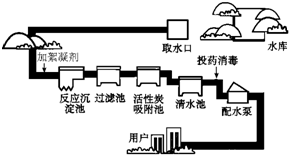 人类生活和工业农业生产都离不开水.下图是自来水厂净水过程的示意图.请根据图示回答问题:
人类生活和工业农业生产都离不开水.下图是自来水厂净水过程的示意图.请根据图示回答问题: