��Ŀ����
�±����Ȼ��ƺ�̼�����ڲ�ͬ�¶�ʱ���ܽ�ȣ����ݴ˱��ش�
�¶�/�� | 10 | 20 | 30 | 40 | |
�ܽ��/g | �Ȼ��� | 35.8 | 36.0 | 36.3 | 36.6 |
̼���� | 12.2 | 21.8 | 39.7 | 53.2 | |
��1��40��ʱ���Ȼ��Ƶ��ܽ��Ϊ________g��
��2��̼������Һ�л����������Ȼ��ƣ���ͨ��________�ᾧ�����ᴿ��
��3����20��ʱ����100gˮ�м���25 g̼���ƣ���ֽ����õ�����_____������͡������͡�����Һ����������Һ���µ�30�棬������Һ��������������Ϊ________��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���ͳ�ƣ��ҹ�ÿ�걨�ϵ��ֻ�����1�ڲ����������л������ã�����ɾ���˷Ѻ���Ⱦ��ͬѧ�ǶԷϾ��ֻ��еĽ������ղ�����Ȥ��
��������⡿ �ӷϾ��ֻ��п��Ի��յ���Щ�м�ֵ�Ľ�������λ��գ�
���������ϡ�
���ֻ���·���еĽ�������۸����±���ʾ��
���� | Fe | Cu | Al | Ni | Au | Ag | Pd���٣� |
�г��۸�/��$/t�� | 3 6 5 | 7175.5 | 1710.5 | 1 4 2 3 5 | 4.7��107 | 7.6��105 | 2 . 7 �� 1 0 7 |
��ʯ�к��� | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
�ֻ���·���к��� | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
˵����Fe��Cu��Al��Ni�ĺ���������������%����ʾ��Au��Ag��Pd�ĺ����ĵ�λΪ��g/t����
��Ni�Ľ������λ����ǰ��Pd�Ľ������λ����� NiCl2��ҺΪ��ɫ��
��2Cu + O2 + 2H2SO4  2CuSO4 + 2H2O
2CuSO4 + 2H2O
��ʵ�鷽����
��һ����ѡ��ֵ�û��յĽ���
�������Ϣ��е����ݣ��Ͼ��ֻ����л��ռ�ֵ�Ľ�����Au��Ag��Cu��Pd��ԭ���ǣ�
�� _____________�������ǵ��г��۸�ϸߡ�
�ڶ��������ʵ����롢���ղ��ֽ���
��� | ʵ�鲽�� | ʵ������ |
I | ȡһ�Ͼ��ֻ���·�壬�õ紵���������·���ӵ�ĺ������ȷ磬һ��ʱ��������ӽ�������·�����ϰ���ק�� | �����ۻ� |
II | ��������·�����ձ��У��������ϡ������� | ���� |
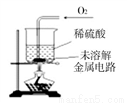
III | ȡII��δ�ܽ�Ľ�����·��������ˮϴ��������ͼ��ʾװ���У�����ʵ�顣 | ��Һ�����ɫ����������������δ�ܽ� |
IV | ����III���ձ��е����ʣ�ϴ����ֽ�ϵ����� | ��ֽ���������������� |
V | ���� | ���� |
���������ۡ�
��1���ɲ���I�е�������֪�ĺ���������������____________��
��2������II��Ӧ��ʵ��������___________��
��3������II������Һ�У����ٺ���������_____________�֡�
��4������V�IJ����ǣ�������������Һ�м���һ�������ۡ�������ʵ����̼�������ǰ����Һ����Ҫ���ӱ仯ʾ��ͼ����ͼ��ʾ��
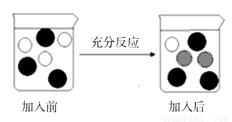
�� ͼ�С� �����������ķ���Ϊ____________��
�����������ķ���Ϊ____________��
�� ��ַ�Ӧ����ˣ���ֽ�Ϲ���������____________��д��ѧʽ����
��һ�λ�ѧʵ���У�ͬѧ�ǽ���������ͭ��Һ��μӵ�5mL��������������Һ�У��۲쵽�����쳣ʵ������
ʵ����� | �μ�����ͭ��Һ���� | ʵ������ |
�� | ��1��6�� | ������ɫ���������������ʧ���γ�����ɫ��Һ |
�� | ��7��9�� | ������ɫ�������ҳ��������࣮���������ʧ���ܿ�������ɫ |
��ʵ�����ͬѧ�Ǹ�����ѧ���л�ѧ֪ʶ�ж���ɫ�����Ļ�ѧʽ��_____________������д��������ɫ�����Ļ�ѧ����ʽ___________________��
ʵ�������ɫ����Ϊʲô��ʧ��ͬѧ�Ǽ�����������̽����
���������ϡ���.������ͭ���������ȶ���70�橁80��ʱ����ˮ�ֽ���������ͭ
��ͭ���ƻ�ѧʽ:Na2[Cu(OH)4]����ˮ����Һ������ɫ
�����������ۡ�С����Ϊ��ɫ������ʧ������������ͭ�����˷ֽ⡣����ͬѧһ�·������IJ²⣬������___________________��
ͬѧ�ǽ������ۺ�����������ֲ��롣
����һ������������ͭ����������ˮ�У�
�������������ͭ����������������Ũ��Һ���ܽ⣬��Һ������ɫ��
��ʵ��̽����Ϊ��֤���룬ͬѧ����������ͭ��ĩ�������Լ�����ѡ���������ʵ�顣������д���еĿո�
ʵ����� | ʵ�鷽������� | ʵ������ | ���� |
�� | ������������ͭ��ĩ�ӵ�5mL����ˮ�У������ | ________ | ����һ���� |
�� | ____________ | ________ | �������ȷ |
�������뷴˼��
��1������ʵ�飬����������֪����������ͭ������������Һ���ܽ�����Na2[Cu(OH)4]���÷�Ӧ�Ļ�ѧ����ʽ��___________________��
��2������ʵ���֪��������ͭ��Һ�뱥������������Һ�ķ�Ӧ�Ƿ��ȷ�Ӧ�����ݵ�ʵ��������____________________��