题目内容
现有10%的NaCl溶液、10%的稀盐酸、20%的盐酸、10%氢氧化钠溶液、20%的氢氧化钠溶液,现将这五种溶液编号为A、B、C、D、E,则这五种溶液的pH由小到大的顺序是 .
考点:溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:根据已有的知识进行分析,氯化钠的溶液呈中性,pH等于7,盐酸呈酸性,pH小于7,且溶液的溶质质量分数越大,酸性越强,pH越小;氢氧化钠溶液呈碱性,pH大于7,且溶液的溶质质量分数越大,碱性越强,pH越大,据此解答.
解答:解:氯化钠的溶液呈中性,pH等于7;盐酸呈酸性,pH小于7,且溶液的溶质质量分数越大,酸性越强,pH越小,故10%的稀盐酸的pH大于20%的盐酸的pH;氢氧化钠溶液呈碱性,pH大于7,且溶液的溶质质量分数越大,碱性越强,pH越大,故10%氢氧化钠溶液小于20%的氢氧化钠溶液的pH,故其pH由小到大的顺序为20%的盐酸、10%的稀盐酸、10%的NaCl溶液、10%氢氧化钠溶液、20%的氢氧化钠溶液,故填:C、B、A、D、E.
点评:本题考查了溶液的酸碱性于pH的关系,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
新闻链接:2014年02月04日22时许,沈阳市黄姑区华山路一小区,34岁的李先生带着4岁的龙凤胎宝宝燃放爆竹,结果爆竹引燃了化粪池内沼气,发生爆炸.其实化粪池里产生有较大量的沼气,其主要成分就有CH4.下列有关说法不正确的是( )
| A、不应该建化粪池 |
| B、化粪池周围禁放烟花爆竹 |
| C、甲烷充分燃烧生成CO2和H2O |
| D、甲烷是可燃性气体 |


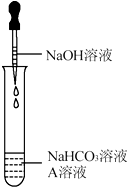 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应. 我们学习化学的目的之一就是学会从化学的视角认识和分析生活生产中的一些问题.
我们学习化学的目的之一就是学会从化学的视角认识和分析生活生产中的一些问题.

 ,则y=
,则y=