题目内容
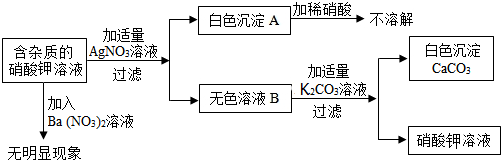
17.常见的食品脱氧剂多为无机铁系脱氧剂(各成分比2g铁粉、0.5g活性炭、0.5g食盐),其主要成分为活性铁粉.某同学充满好奇,想提取脱氧剂的成分活性炭进行后续实验:具体步骤流程如下,请回答:步骤Ⅰ:

步骤Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如图(部分产物略去)

(1)操作Ⅰ的名称是过滤,溶液丙中含有的溶质是FeSO4、NaCl、H2SO4(写化学式);
(2)固体乙在反应①中体现出的用途是冶炼金属.(填:作燃料、冶炼金属)
(3)反应②的基本类型是置换反应,A与C完全反应后,溶液D的颜色是浅绿色.
(4)写出符合反应③的化学方程式为:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
分析 (1)过滤可以把不溶于水的物质除去;根据反应过程可以判断溶液中的溶质;
(2)固体乙为活性炭,固体乙在反应①中体现出的用途是与金属氧化物发生置换反应,生成金属单质;
(3)反应②是铁与硫酸铜反应;
(4)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
解答 解:(1)操作Ⅰ的名称是过滤;溶液丙中含有的溶质有:反应生成的硫酸亚铁,原来的氯化钠,还有没有反应的硫酸;
(2)固体乙为活性炭,固体乙在反应①中体现出的用途是与金属氧化物发生置换反应,生成金属单质;
(3)反应②是铁与硫酸铜反应生成铜与硫酸亚铁,为置换反应,溶液D为硫酸亚铁溶液,为浅绿色;
(4)硫酸铜和氢氧化钠反应能生成氢氧化铜沉淀和硫酸钠,反应的化学方程式分别为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
故答案为:(1)过滤;H2SO4、NaCl、FeSO4;
(2)冶炼金属;
(3)置换反应,浅绿色;
(4)CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
点评 本题主要考查实验探究方面的知识,解答时要掌握物质之间相互作用时的反应情况,特别是要能够根据物质的性质方面的知识来判断具体的物质,并且能够根据质量守恒定律的内容正确的书写反应的化学方程式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.分类是化学学习过程中常用的方法,下列分类中正确的是( )
| A. | 合成材料:涤纶、塑料、玻璃 | |
| B. | 氧化物:生石灰、铁锈、二氧化锰 | |
| C. | 合金:生铁、锰钢、青铜 | |
| D. | 复合肥料:磷酸二氢钙、尿素、硝酸钾 |
12.20℃时,KNO3的溶解度为31.6g.此温度下,在100g水中形成的KNO3溶液的叙述中,不正确的是( )
| A. | 饱和溶液的容剂质量是100g | B. | 不饱和溶液的容剂质量是100g | ||
| C. | 饱和溶液的容剂质量是31.6g | D. | 不饱和溶液的容剂质量是31.6g |
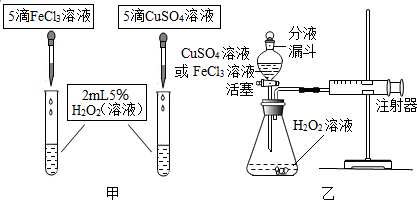
9.为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
(1)请写出H2O2分解的化学方程式:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
【定性探究】
(2)如图甲,可通过观察产生气泡的速率来定性比较两者的催化效果.
【定量探究】
(3)如图乙,实验前检查该装置的气密性的方法是将注射器活塞向外拉,再松开手活塞又回到原来的位置,则装置气密性良好.要定量比较两者的催化效果,可测量生成等体积气体所需的时间.
【深入探究】
(4)在FeCl3溶液中,究竟是哪种离子起催化作用呢?
猜想1:铁离子(Fe3+)起催化作用;
猜想2:氯离子(Cl-)起催化作用;
…
请设计实验,验证猜想1

(1)请写出H2O2分解的化学方程式:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
【定性探究】
(2)如图甲,可通过观察产生气泡的速率来定性比较两者的催化效果.
【定量探究】
(3)如图乙,实验前检查该装置的气密性的方法是将注射器活塞向外拉,再松开手活塞又回到原来的位置,则装置气密性良好.要定量比较两者的催化效果,可测量生成等体积气体所需的时间.
【深入探究】
(4)在FeCl3溶液中,究竟是哪种离子起催化作用呢?
猜想1:铁离子(Fe3+)起催化作用;
猜想2:氯离子(Cl-)起催化作用;
…
请设计实验,验证猜想1
| 实验操作 | 实验现象 | 实验现象 |
| 分别取某体积的同种H2O2溶液于2支试管中,再分别加入等质量的FeCl3和NaCl | 加入FeCl3的试管中产生的气体快,加入NaCl的试管中产生的气体慢 | 猜想1成立 |
7.生石灰是一种传统的建筑材料,俗称“石灰”.工业上通过在石灰窑中煅烧石灰石制得“石灰”,其反应原理是:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.兴趣小组的同学对某地刚出窑的“石灰”的成分进行探究.
【提出问题】
刚出窑的“石灰”有那些成分?
【猜想】
I.只有氧化钙Ⅱ.只有碳酸钙ⅢI.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想 II成立.乙同学认为上述实验不足以证明猜想 II成立,其理由是沉淀也可能是未溶解的氢氧化钙,有白色不溶物只能说明样品可能有碳酸钙,不能说明 II.只有碳酸钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量,几滴稀盐酸和氢氧化钙反应,没有和碳酸钙反应.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告.
【思考】使用“石灰”的建筑工地上常有一个大的石灰池,使用“石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用.长期使用的石灰池内壁会逐渐增厚,其主要原因是氢氧化钙吸收空气中的二氧化碳形成难溶的碳酸钙.
【提出问题】
刚出窑的“石灰”有那些成分?
【猜想】
I.只有氧化钙Ⅱ.只有碳酸钙ⅢI.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想 II成立.乙同学认为上述实验不足以证明猜想 II成立,其理由是沉淀也可能是未溶解的氢氧化钙,有白色不溶物只能说明样品可能有碳酸钙,不能说明 II.只有碳酸钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量,几滴稀盐酸和氢氧化钙反应,没有和碳酸钙反应.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品加水溶解滴加酚酞 ②取样品滴加稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅲ成立 |
 配制50g5%氯化钠溶液.回答问题:
配制50g5%氯化钠溶液.回答问题: