题目内容
(1)小刚同学为了学好化学,备有一个错题记录本,用于失误诊断与思维纠偏.下表是他记录的几个错误观点,请你仿照表中示例各找出一个化学方程式来否定相应的错误观点.
(2)小强同学在向盐酸中逐滴滴入氢氧化钠溶液的过程中,多次测定溶液的pH,并据此画出图3的曲线,请回答下列问题:
①图中a点表示______;
②发生反应的化学方程式为______.
| 错 误 观 点 | 否定例证(用化学方程式表示) | ||||
| 示例:氧化反应一定是化合反应 | CH4+2O2
| ||||
| 化合反应中的反应物都是单质 | |||||
| 复分解反应中一定要有沉淀生成 |
①图中a点表示______;
②发生反应的化学方程式为______.

(1)化合反应是两种或两种以上物质生成一种物质的反应,反应物不一定都是单质,如氧化钙和水反应,反应的方程式:CaO+H2O=Ca(OH)2;
复分解反应的条件是;有沉淀或气体或水生成,生成物可能有沉淀,但不一定有沉淀生成,例如盐酸和氢氧化钠反应生成氯化钠和水,反应的方程式为:NaOH+HCl=NaCl+H2O.
(2)根据pH=7可知,溶液显中性,说明盐酸和氢氧化钠恰好反应生成氯化钠和水,反应的方程式为:NaOH+HCl=NaCl+H2O.
故答案为:(1)CaO+H2O=Ca(OH)2;NaOH+HCl=NaCl+H2O.
(2)①盐酸和氢氧化钠恰好反应生成氯化钠和水;②NaOH+HCl=NaCl+H2O.
复分解反应的条件是;有沉淀或气体或水生成,生成物可能有沉淀,但不一定有沉淀生成,例如盐酸和氢氧化钠反应生成氯化钠和水,反应的方程式为:NaOH+HCl=NaCl+H2O.
(2)根据pH=7可知,溶液显中性,说明盐酸和氢氧化钠恰好反应生成氯化钠和水,反应的方程式为:NaOH+HCl=NaCl+H2O.
故答案为:(1)CaO+H2O=Ca(OH)2;NaOH+HCl=NaCl+H2O.
(2)①盐酸和氢氧化钠恰好反应生成氯化钠和水;②NaOH+HCl=NaCl+H2O.

练习册系列答案
相关题目
王老师在化学课上经常组织同学们开展一些探究活动:
(1)有一次王老师刚说为了探究酸的通性,需要先将浓硫酸稀释成稀硫酸.小明就立刻自告奋勇上台说要来完成这项稀释工作,王老师对他的学习热情给予了高度评价,不过当他用大量筒量取好20mL浓硫酸后,正准备将水加入到量筒中时,王老师立即进行了制止,并说他犯了两个原则性错误.请你写出小明的这两个错误;.
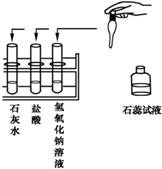
(2)一次王老师让甲、乙两组同学分别做常见酸和碱与指示剂反应的实验,所做的实验和使用的试剂如右图所示.实验后废液分别集中倒进各组的废液缸时,发现甲组废液呈红色,乙组废液呈蓝色.
请你分析废液的成分:甲组废液可能含有;
乙组废液中可能含有.
假如将甲组的废液直接排入铸铁管下水道,会造成什么危害?
答:.
(3)自然界的物质每时每刻都在发生着各种各样的变化,而这些变化不仅与物质的性质有关,还与外界条件密不可分.因此人们利用这其中的规律,就可在生产、生活和科学实验中,通过控制条件来控制化学反应的发生.王老师要同学们结合初中化学已学过的知识,来说明以下问题:

(1)有一次王老师刚说为了探究酸的通性,需要先将浓硫酸稀释成稀硫酸.小明就立刻自告奋勇上台说要来完成这项稀释工作,王老师对他的学习热情给予了高度评价,不过当他用大量筒量取好20mL浓硫酸后,正准备将水加入到量筒中时,王老师立即进行了制止,并说他犯了两个原则性错误.请你写出小明的这两个错误;.
(2)一次王老师让甲、乙两组同学分别做常见酸和碱与指示剂反应的实验,所做的实验和使用的试剂如右图所示.实验后废液分别集中倒进各组的废液缸时,发现甲组废液呈红色,乙组废液呈蓝色.
请你分析废液的成分:甲组废液可能含有;
乙组废液中可能含有.
假如将甲组的废液直接排入铸铁管下水道,会造成什么危害?
答:.
(3)自然界的物质每时每刻都在发生着各种各样的变化,而这些变化不仅与物质的性质有关,还与外界条件密不可分.因此人们利用这其中的规律,就可在生产、生活和科学实验中,通过控制条件来控制化学反应的发生.王老师要同学们结合初中化学已学过的知识,来说明以下问题:
| 相关结论 | 能说明此结论的实验事实 |
| ①反应物浓度越大,反应越强烈 | |
| ②温度不同,反应发生的情况不同 | |
| ③有些变化受两个或两个以上条件控制,缺一不可. |

 25、王老师在化学课上经常组织同学们开展一些探究活动:
25、王老师在化学课上经常组织同学们开展一些探究活动:


