题目内容
18. 早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用如图装置进行实验探究,请按要求填空:(1)写出CO还原Fe2O3的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)实验中盛澄清石灰水的试管中可观察到的现象是石灰水变浑浊,反应的方程式是CO2+Ca(OH)2═CaCO3↓+H2O;
(3)右边导气管口放置点燃的酒精灯的目的是进行尾气处理,防止污染空气;
(4)实验结束时,应当先停止加热,后继续通入一氧化碳直到试管冷却,这样做的目的是防止铁再次被氧化.
分析 根据已有的知识进行分析解答,一氧化碳能与氧化铁在高温下反应生成铁和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,一氧化碳是有毒的气体,需要进行尾气处理,据此解答.
解答 解:(1)一氧化碳能与氧化铁在高温下反应生成铁和二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)二氧化碳能使澄清的石灰水变浑浊,故可以观察到石灰水变浑浊的现象,二氧化碳能使澄清的石灰水变浑浊,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;故填:石灰水变浑浊;
CO2+Ca(OH)2═CaCO3↓+H2O;
(3)一氧化碳是有毒的气体,排放到空气中会污染空气,利用一氧化碳的可燃性采用点燃的方法处理一氧化碳,可以防止污染空气,故填:进行尾气处理,防止污染空气;
(4)试验结束后,应当先停止加热,继续通入一氧化碳直到试管冷却,防止铁再次被氧化.答案:停止加热;继续通入一氧化碳直到试管冷却;防止铁再次被氧化.’
点评 本题考查的是一氧化碳还原氧化铁实验以及实验的注意事项,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
2.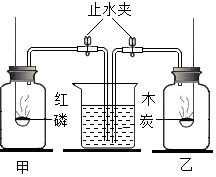 如图所示,等体积的甲乙两集气瓶内充满空气,燃烧匙里分别盛有过量的红磷和木炭,点燃使其充分反应,冷却至室温,打开止水夹,观察到的现象是( )
如图所示,等体积的甲乙两集气瓶内充满空气,燃烧匙里分别盛有过量的红磷和木炭,点燃使其充分反应,冷却至室温,打开止水夹,观察到的现象是( )
 如图所示,等体积的甲乙两集气瓶内充满空气,燃烧匙里分别盛有过量的红磷和木炭,点燃使其充分反应,冷却至室温,打开止水夹,观察到的现象是( )
如图所示,等体积的甲乙两集气瓶内充满空气,燃烧匙里分别盛有过量的红磷和木炭,点燃使其充分反应,冷却至室温,打开止水夹,观察到的现象是( )| A. | 甲瓶没有水流入,乙瓶有水流入 | B. | 甲乙两瓶均有水流入 | ||
| C. | 甲瓶有水流入,乙瓶没有 | D. | 甲乙两瓶均没有 |
8.X的化学式为( )
| A. | CrO3 | B. | K2CrO7 | C. | K2Cr2O7 | D. | K2CrO4 |