题目内容
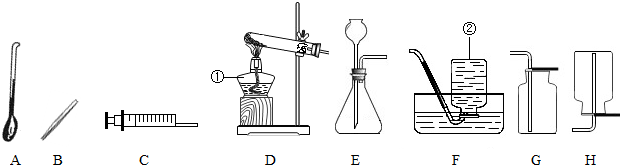
请根据如图装置回答下列问题:
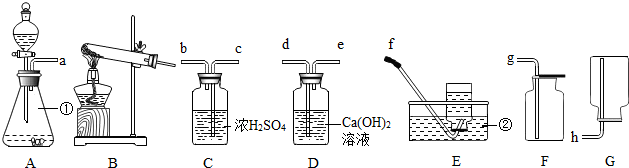
(1)写出有标号的仪器名称:① ,② .
(2)若要制取氧气,应选择的发生装置是 ,收集装置是 ,发生的化学反应为 .
(3)若要用上述装置制取CO2,则选择的发生装置是 ,化学反应为 ;若收集一瓶干燥的CO2气体,其装置的连接顺序是 (用接口字母从左到右顺序连接).
(4)若要制氢气,选择的发生装置是 ,收集装置是 ,发生的化学反应是 .

(1)写出有标号的仪器名称:①
(2)若要制取氧气,应选择的发生装置是
(3)若要用上述装置制取CO2,则选择的发生装置是
(4)若要制氢气,选择的发生装置是
考点:常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),实验室制取氧气的反应原理,二氧化碳的实验室制法,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)据常用仪器回答;
(2)实验室制取氧气可用常温分解过氧化氢的方法,属于固液常温型,可选发生装置A,还可用加热高锰酸钾、或加热氯酸钾和二氧化锰混合物的方法,属于固体加热型,可选发生装置B,氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,并据反应原理书写方程式;
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,属于固液常温型,故选发生装置A,并据反应原理书写方程式,收集一瓶干燥的CO2气体,则气体先通入浓硫酸干燥,二氧化碳密度比空气大,用向上排空气法,洗气装置导管要长进短出,据此确定导管连接顺序;
(4)实验室制取氢气用锌和稀硫酸反应,不需加热,属于固液常温型,故选发生装置A,氢气密度比空气小,难溶于水,所以可用向下排空气法或排水法收集,并据反应原理书写方程式.
(2)实验室制取氧气可用常温分解过氧化氢的方法,属于固液常温型,可选发生装置A,还可用加热高锰酸钾、或加热氯酸钾和二氧化锰混合物的方法,属于固体加热型,可选发生装置B,氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,并据反应原理书写方程式;
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,属于固液常温型,故选发生装置A,并据反应原理书写方程式,收集一瓶干燥的CO2气体,则气体先通入浓硫酸干燥,二氧化碳密度比空气大,用向上排空气法,洗气装置导管要长进短出,据此确定导管连接顺序;
(4)实验室制取氢气用锌和稀硫酸反应,不需加热,属于固液常温型,故选发生装置A,氢气密度比空气小,难溶于水,所以可用向下排空气法或排水法收集,并据反应原理书写方程式.
解答:解:(1)标号仪器分别是锥形瓶、水槽;
(2)实验室制取氧气可用常温分解过氧化氢的方法,属于固液常温型,可选发生装置A,还可用加热高锰酸钾、或加热氯酸钾和二氧化锰混合物的方法,属于固体加热型,可选发生装置B,氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应方程式是2H2O2
2H2O+O2↑,氯酸钾在加热、二氧化锰作催化剂的条件下生成氯化钾和氧气,反应方程式是:2KClO3
2KCl+3O2↑、加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是:2KMnO4
K2MnO4+MnO2+O2↑;
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,属于固液常温型,故选发生装置A,大理石主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O,收集一瓶干燥的CO2气体,则气体先通入浓硫酸干燥,二氧化碳密度比空气大,用向上排空气法,洗气装置导管要长进短出,所以导管连接顺序是a→d→e→c;
(4)实验室制取氢气用锌和稀硫酸反应,不需加热,属于固液常温型,故选发生装置A,氢气密度比空气小,难溶于水,所以可用向下排空气法或排水法收集,锌和硫酸反应生成硫酸锌和氢气,反应方程式是Zn+H2SO4=ZnSO4+H2↑;
故答案为:(1)锥形瓶;水槽;
(2)A(或B);E(或F);2H2O2
2H2O+O2↑(或2KClO3
2KCl+3O2↑、2KMnO4
K2MnO4+MnO2+O2↑);
(3)A;CaCO3+2HCl═CaCl2+H2O+CO2↑;a→d→e→c;
(4)B;E(或G);Zn+H2SO4=ZnSO4+H2↑.
(2)实验室制取氧气可用常温分解过氧化氢的方法,属于固液常温型,可选发生装置A,还可用加热高锰酸钾、或加热氯酸钾和二氧化锰混合物的方法,属于固体加热型,可选发生装置B,氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应方程式是2H2O2
| ||
| ||
| △ |
| ||
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,属于固液常温型,故选发生装置A,大理石主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O,收集一瓶干燥的CO2气体,则气体先通入浓硫酸干燥,二氧化碳密度比空气大,用向上排空气法,洗气装置导管要长进短出,所以导管连接顺序是a→d→e→c;
(4)实验室制取氢气用锌和稀硫酸反应,不需加热,属于固液常温型,故选发生装置A,氢气密度比空气小,难溶于水,所以可用向下排空气法或排水法收集,锌和硫酸反应生成硫酸锌和氢气,反应方程式是Zn+H2SO4=ZnSO4+H2↑;
故答案为:(1)锥形瓶;水槽;
(2)A(或B);E(或F);2H2O2
| ||
| ||
| △ |
| ||
(3)A;CaCO3+2HCl═CaCl2+H2O+CO2↑;a→d→e→c;
(4)B;E(或G);Zn+H2SO4=ZnSO4+H2↑.
点评:本题考查了常见气体的实验室制法的原理和发生装置、收集方法选择,并熟练掌握常见的仪器的用途和名称,是初中阶段的重点内容,也是中考的必考知识点,要求学生在理解的基础上要学会举一反三.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
鉴别H2、N2和空气,最好的方法是( )
| A、观察其颜色和状态 |
| B、嗅其气味 |
| C、用燃着的木条分别检验 |
| D、用带火星的木条分别检验 |
下列过程涉及到的变化主要是化学变化的是( )
| A、过滤 | B、石油分馏 |
| C、煤隔绝空气加强热 | D、海水晒盐 |
某工厂的废渣中有少量的锌粉和氧化铜,跟大量盐酸形成的污水,产生公害,若向污水中放入铁粉,且反应后铁粉有剩余,此时污水中一定含有的金属离子是( )
| A、Fe2+ Cu2+ |
| B、Cu2+ H+ |
| C、Zn2+ Fe2+ |
| D、Zn2+ H+ |
下列实验操作中不正确的是( )
A、 点燃酒精灯 |
B、 测定空气里氧气含量 |
C、 取用炭粉 |
D、 验满气体 |