题目内容
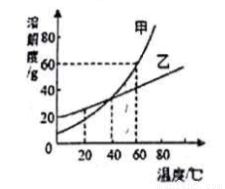
将等质量的镁、铁、锌分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2的质量与反应时间的关系如图所示.根据图中的信息,作出的判断不正确的是( )

A. 图线X表示镁的反应情况
B. 铁消耗的稀盐酸的质量最大
C. 镁、锌一定过量,铁可能反应完
D. 镁一定过量,锌、铁可能反应完
【答案】C
【解析】试题分析:根据金属活动性顺序可知A、图中X反应速度最快,说明X是三种金属中活动性最强的镁;所以判断正确; B、图中铁生成氢气最多,根据反应前后元素质量不变,可判断铁消耗盐酸质量最大;所以判断正确; C、图中镁、锌产生氢气质量相等,说明镁没有完全反应,但不能确定锌也没有完全反应;所以判断错误; D、质量相等的锌、铁完全反应产生氢气的质量关系为:铁>锌,与图中关系一致,可推测锌、铁可能完全反应.所以判断正确;故选C.
考点:金属的性质、金属活动性顺序
【题型】单选题
【结束】
30
向AgNO3溶液中加入一定量的Mg粉和Cu粉,充分反应后过滤,得到滤渣和蓝色的滤液.关于该滤渣和滤液有下列四种说法:①向滤渣中加入稀盐酸,可能有气泡产生;②向滤液中加入稀盐酸一定有沉淀产生;③滤渣中一定有Ag;④滤液中一定有Cu(NO3)2、一定不含AgNO3、可能有Mg(NO3)2,以上说法中正确的个数为( )
A. 1个 B. 2个 C. 3个 D. 4个
【答案】A
【解析】①充分反应后过滤,得到滤渣和蓝色的滤液,说明镁已经完全反应,铜和硝酸银反应生成了硝酸铜,向滤渣中加入稀盐酸,不可能有气泡产生,错误;②铜和硝酸银反应时,如果硝酸银有剩余,向滤液中加入稀盐酸一定有沉淀产生,如果硝酸银没有剩余,则向滤液中加入稀盐酸没有沉淀产生,错误;③滤渣中一定有Ag,正确;④滤液中一定有Cu(NO3)2、可能含AgNO3、一定有Mg(NO3)2,错误。故选A。
【题型】null
【结束】
31
化学来源于生活,服务于杜会,在生活中蕴藏着许多化学知识。
(1)石家庄市已完成“天然气置换工程”,用天然气代替煤气更有利于保护环境,请写出天然气燃烧的化学方程式____;
(2)“共享单车”由于符合“低碳出行”的理念,现已风靡石家庄,尤其颇受年轻人的喜爱,“低碳出行”中“低碳“指的是较低的______气体排放:如下图所示自行车中的材料属于金属材料的是______(选填序号①、②、③),为防止“共享单车”钢丝网篓锈蚀,可采取的措施有_________(写一种即可)。

(3)碘酒杀菌中的的“酒”指________(用化学式表示);
(4)用洗洁精洗去餐具上的油污,是利用了洗洁精的______作用。
下图表示有关物质的转化关系(反应条件及部分生成物已省略)。已知甲、乙、丙为单质,其它均为化合物,A、C都是无色液体,且所含元素种类完全相同:D是无色有毒气体。
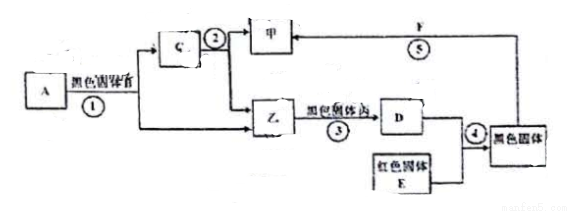
(1)F的化学式可能为(填一个即可)________。
(2)反应②的化学方程式________。
(3)反应④的化学方程式__________。
(4)反应①-⑤中属于分解反应的是_______________(填序号)。
(5)反应⑤的现象为___________。
【答案】 HCl或H2SO4 2H2O 2H2↑+O2↑
2H2↑+O2↑  ①②色 有气泡产生,溶液由无色变为浅绿、黑色固体减少
①②色 有气泡产生,溶液由无色变为浅绿、黑色固体减少
【解析】本题是推断题,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证。
A与C的组成元素相同的液体,乙为单质,可判断A为过氧化氢、 C为水,乙为氧气;由C分解生成氧气和甲,则甲是氢气;根据丙为黑色粉末且D是无色有毒气体,丙是碳,则D是一氧化碳;一氧化碳与红色固体E反应生成黑色固体,则红色固体为氧化铁,黑色固体是铁,铁能与酸溶液反应生成氢气 ,则F为酸溶液,可能为稀硫酸或稀盐酸,代入框图,假设合理。因此:
(1)F是硫酸或盐酸,化学式为HCl或H2SO4;
(2)反应②是水在通电条件下生成了氧气和氢气,化学方程式是2H2O 通电 2H2↑+ O2 ↑ ;
(3)反应④是一氧化碳和氧化铁在高温条件下生成了二氧化碳和铁,化学方程式是 ;
;
(4)反应①-⑤中①②都是由一种物质生成两种物质,属于分解反应;。
(5)反应⑤是铁与酸溶液反应的现象为有气泡产生,溶液由无色变为浅绿色,黑色固体减少
。
【题型】推断题
【结束】
35
小明过生日,吹蜡烛时怎么吹也吹不灭,小明同学带着疑问与化学兴趣小组的老师和同学一起对“吹不灭的蜡烛”展开了探究。
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末,打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃,当蜡烛吹灭后,未冷却的金属继续燃烧,从而使蜡烛复燃。吹不灭的蜡烛芯外的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,他们进行了下面的探究。(不考虑打火石中稀土元素对探究金属性质的影响)
【提出问题】“吹不灭蜡烛”打火石中含有哪种金属?
【做出猜想】
猜想一:该金属是Cu 猜想二:该金属是Fe
猜想三:该金属是Mg 猜想四:该金属是Al
【实验探究】同学们根据所学的化学知识设计并进行如下实验确定该金属的成分.
(1)甲同学切开蜡烛,取出打火石,用砂纸打磨,打火石呈银白色,猜想一不成立,原因是_________。
(2)乙同学取少量打磨后的打火石于试管中,滴加稀盐酸,观察现象,经过对现象的分析后,他们认为该金属一定不是铁,他们观察到的现象是_______,猜想二不成立。
(3)为了进一步确定该金属的种类,小明提议用硫酸铜溶液进行试验,请你预测,将打火石加入到硫酸铜溶液后的现象是__________,其中涉及到的化学方程式______________。(任写一个即可)
(4)同学们一致认为小明的方案不合理,经过讨论他们设计了下面的实验方案,确认了打火石中的金属是镁。
操作步骤 | 实验现象 | 实验结论 |
取一块打磨后的“打火石”于试管中,加入少量__________溶液 | “打火石”表面有银白色固体析出 | “打火石”中的金属是Mg |
有关的化学方程式为_______________________。
【交流与反思】这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?_______________,
这种蜡烛实际也可以熄灭,可采用的方法是_____________(填一种即可)。
【答案】 铜为紫红色 溶液为无色 打火石表面有红色固体附着,溶液颜色变浅(或变为无色) Mg+CuSO4=MgSO4+Cu或2Al+3CuSO4=Al2(SO4)3+3Cu(任写一个即可) 硫酸铝 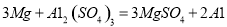 蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以然烧 隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)
蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以然烧 隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)
【解析】本题考查了金属的性质和物质燃烧的条件。
(1)甲同学切开蜡烛,取出打火石,用砂纸打磨,打火石呈银白色,猜想一不成立,原因是铜为紫红色;
(2)铁与稀盐酸反应会生成浅绿色溶液。乙同学取少量打磨后的打火石于试管中,滴加稀盐酸,观察现象,经过对现象的分析后,他们认为该金属一定不是铁,他们观察到的现象是溶液为无色,猜想二不成立;
(3)铝和镁的活动性都大于铜,都能将硫酸铜中铜置换出来,生成硫酸铝或硫酸镁,所以可预测,将打火石加入到硫酸铜溶液后的现象是打火石表面有红色固体附着,溶液颜色变浅(或变为无色),其中涉及到的化学方程式2Al+3CuSO4=Al2(SO4)3+3Cu或Mg+CuSO4=MgSO4+Cu;
(4)镁的活动性大于铝,镁能将铝盐溶液中的铝置换出来。取一块打磨后的“打火石”于试管中,加入少量硫酸铝溶液,该反应是镁与硫酸铝反应生成硫酸镁和铝,化学方程式是: 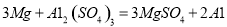 ;蜡烛芯里的金属不燃烧原因是蜡烛烛芯被石蜡蒸汽包围着,缺少氧气里面的金属难以然烧;熄灭蜡烛可采用的方法是隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)。
;蜡烛芯里的金属不燃烧原因是蜡烛烛芯被石蜡蒸汽包围着,缺少氧气里面的金属难以然烧;熄灭蜡烛可采用的方法是隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)。
【题型】科学探究题
【结束】
36
某化学兴趣小组同学为回收一块质量为40 g的铜锌合金中的铜,将该合金放人烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100 g,烧杯内剩余固体27 g。请完成下列计算:
(1)40 g铜锌合金中锌的质量是________g 。
(2)计算所用稀硫酸中溶质的质量分数为_________。


 ),完全反应后可生成5.6t生石灰(
),完全反应后可生成5.6t生石灰( )固体和二氧化碳气体(已知石灰石中的杂质都是固体且都不参与反应)。试计算:
)固体和二氧化碳气体(已知石灰石中的杂质都是固体且都不参与反应)。试计算: 中钙元素与氧元素的质量比(最简整数比)。
中钙元素与氧元素的质量比(最简整数比)。 B.
B.  C.
C.  D.
D.