题目内容
某化学兴趣小组用下图所示装置进行制取气体实验,请你回答有关问题:
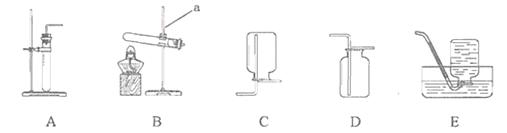
(1)实验仪器a的名称是______________。
(2)甲同学用MnO2和H2O2来制取氧气,应选择的发生装置和收集装置是 ,
MnO2固体在该反应中起____ __作用。
(3)氨气(NH3)是一种无色、有刺激性气味,极易溶于水,密度比空气小的气体。乙
同学用加热熟石灰和氯化铵(均为固体)的方法来制取氨气,乙同学应选择制取氨气的发
生装置和收集装置是 。
(4)丙同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,该反应的文字表达式为____ ___。实验时应在试管口放一团棉花,其作用是 ;用排水法收集氧气的合适时机是 ,检验气体是O2的方法是__________________________________。实验结束时,发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2
做出上述猜想的理由是_____ __。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想____________错误。
②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法就得出了猜想Ⅱ是正确的结论。其理由是________________ _ 。
(5)实验结束后,对实验仪器进行清洗。大试管清洗干净的标志是 。

(1)实验仪器a的名称是______________。
(2)甲同学用MnO2和H2O2来制取氧气,应选择的发生装置和收集装置是 ,
MnO2固体在该反应中起____ __作用。
(3)氨气(NH3)是一种无色、有刺激性气味,极易溶于水,密度比空气小的气体。乙
同学用加热熟石灰和氯化铵(均为固体)的方法来制取氨气,乙同学应选择制取氨气的发
生装置和收集装置是 。
(4)丙同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,该反应的文字表达式为____ ___。实验时应在试管口放一团棉花,其作用是 ;用排水法收集氧气的合适时机是 ,检验气体是O2的方法是__________________________________。实验结束时,发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2
做出上述猜想的理由是_____ __。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想____________错误。
②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法就得出了猜想Ⅱ是正确的结论。其理由是________________ _ 。
(5)实验结束后,对实验仪器进行清洗。大试管清洗干净的标志是 。
(1) 铁架台 (2) A、E(或A、D);催化 (3)B、C

(4)高锰酸钾 锰酸钾 + 二氧化锰 + 氧气;防止加热时高锰酸钾末进入导管;当气泡均匀连续冒出时;用带火星的木条放在集气瓶口,木条立即复燃;
【提出猜想】它们都是含有氧元素的化合物
【实验验证】Ⅰ;制得了一些氧气
(5)大试管内壁附着的水既不聚集成水滴,也不成股流下。

(4)高锰酸钾 锰酸钾 + 二氧化锰 + 氧气;防止加热时高锰酸钾末进入导管;当气泡均匀连续冒出时;用带火星的木条放在集气瓶口,木条立即复燃;
【提出猜想】它们都是含有氧元素的化合物
【实验验证】Ⅰ;制得了一些氧气
(5)大试管内壁附着的水既不聚集成水滴,也不成股流下。
(1)铁架台是初中常见的实验仪器,实验仪器a的名称是铁架台;
(2)MnO2和H2O2是固体和液体混合且反应条件不需要加热,所以发生装置选择A;氧气的密度大于空气的密度,可用装置D来收集;又因为氧气不易溶于水,可用装置E来收集;MnO2固体在该反应加快了双氧水放出氧气的速率且本身的质量和化学性质不变,作催化剂,起催化作用;
(3)熟石灰和氯化铵均为固体且反应条件为加热,发生装置选择B;氨气极易溶于水,密度比空气小的气体,收集方法选择C;
(4)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应的文字表达式为高锰酸钾 锰酸钾+二氧化锰+氧气;实验时应在试管口放一团棉花,其作用是防止加热时高锰酸钾末进入导管;当气泡均匀连续冒出时,再用排水法收集氧气;氧气具有助燃性,所以检验气体是O2的方法是用带火星的木条放在集气瓶口,木条立即复燃;它们都是含有氧元素的化合物,反应生成的K2MnO4和MnO2分解都有可能放出O2;①由于MnO2的质量不变,猜想Ⅰ错误;②因为实验结果是氧气的实际质量比理论多,既然二氧化锰没有分解放出氧气,那么只有锰酸钾;
锰酸钾+二氧化锰+氧气;实验时应在试管口放一团棉花,其作用是防止加热时高锰酸钾末进入导管;当气泡均匀连续冒出时,再用排水法收集氧气;氧气具有助燃性,所以检验气体是O2的方法是用带火星的木条放在集气瓶口,木条立即复燃;它们都是含有氧元素的化合物,反应生成的K2MnO4和MnO2分解都有可能放出O2;①由于MnO2的质量不变,猜想Ⅰ错误;②因为实验结果是氧气的实际质量比理论多,既然二氧化锰没有分解放出氧气,那么只有锰酸钾;
(5)大试管清洗干净的标志是:大试管内壁附着的水既不聚集成水滴,也不成股流下.
(2)MnO2和H2O2是固体和液体混合且反应条件不需要加热,所以发生装置选择A;氧气的密度大于空气的密度,可用装置D来收集;又因为氧气不易溶于水,可用装置E来收集;MnO2固体在该反应加快了双氧水放出氧气的速率且本身的质量和化学性质不变,作催化剂,起催化作用;
(3)熟石灰和氯化铵均为固体且反应条件为加热,发生装置选择B;氨气极易溶于水,密度比空气小的气体,收集方法选择C;
(4)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应的文字表达式为高锰酸钾
 锰酸钾+二氧化锰+氧气;实验时应在试管口放一团棉花,其作用是防止加热时高锰酸钾末进入导管;当气泡均匀连续冒出时,再用排水法收集氧气;氧气具有助燃性,所以检验气体是O2的方法是用带火星的木条放在集气瓶口,木条立即复燃;它们都是含有氧元素的化合物,反应生成的K2MnO4和MnO2分解都有可能放出O2;①由于MnO2的质量不变,猜想Ⅰ错误;②因为实验结果是氧气的实际质量比理论多,既然二氧化锰没有分解放出氧气,那么只有锰酸钾;
锰酸钾+二氧化锰+氧气;实验时应在试管口放一团棉花,其作用是防止加热时高锰酸钾末进入导管;当气泡均匀连续冒出时,再用排水法收集氧气;氧气具有助燃性,所以检验气体是O2的方法是用带火星的木条放在集气瓶口,木条立即复燃;它们都是含有氧元素的化合物,反应生成的K2MnO4和MnO2分解都有可能放出O2;①由于MnO2的质量不变,猜想Ⅰ错误;②因为实验结果是氧气的实际质量比理论多,既然二氧化锰没有分解放出氧气,那么只有锰酸钾;(5)大试管清洗干净的标志是:大试管内壁附着的水既不聚集成水滴,也不成股流下.

练习册系列答案
相关题目

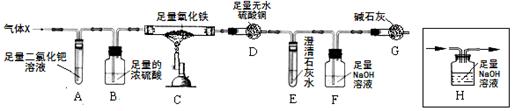
 8Fe +nCO2+2nH2O,其中n的值为 (填数字)。
8Fe +nCO2+2nH2O,其中n的值为 (填数字)。


