题目内容
4.某硫酸厂废水中含有少量硫酸,为达标排放,技术员对废水中的硫酸含量进行了检测.取废水样品100克,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,至10g时恰好完全反应(假设废水其他成分都不与氢氧化钠反应).计算废水中硫酸的质量分数.分析 滴入10g8%的氢氧化钠恰好完全反应,可求反应的氢氧化钠的质量,进而根据氢氧化钠的质量和对应的化学方程式求算稀硫酸中溶质的质量,然后求算其质量分数.
解答 解:
10g质量分数8%的氢氧化钠溶液中氢氧化钠的质量为10g×8%=0.8g
设稀硫酸中溶质的质量为x
2NaOH+H2SO4=Na2SO4+2H2O
80 98
0.8g x
$\frac{80}{98}$=$\frac{0.8g}{x}$
x=0.98g
废水中硫酸的质量分数为$\frac{0.98g}{10g}$×100%=9.8%.
答:废水中硫酸的质量分数为9.8%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
14.下列化学用语表示含义最多的是( )
| A. | 2O | B. | N2 | C. | mAl | D. | Zn2+ |
15.某同学为了测定实验室中氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合,加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如表:
(1)写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)列出求解参加反应的氯酸钾质量(x)的比例式$\frac{245}{96}=\frac{x}{0.96g}$;
(3)求该样品中氯酸钾的纯度98%.
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 2.12 | 2.08 | 2.04 | 2.04 |
(2)列出求解参加反应的氯酸钾质量(x)的比例式$\frac{245}{96}=\frac{x}{0.96g}$;
(3)求该样品中氯酸钾的纯度98%.
12.如图表示家用燃料使用的发展历程(括号内表示主要成分),下列说法正确的是( )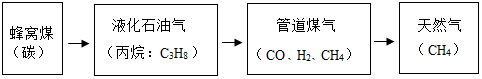

| A. | 煤中主要含有碳元素,是清洁能源 | |
| B. | 煤、石油、天然气和煤气都是化石燃料 | |
| C. | 液化石油气是石油化工的一种产品 | |
| D. | 夜间发现液化气泄露,先开灯进行检查 |
19.如图实验操作正确的是( )
| A. |  倾倒液体 | B. |  稀释浓硫酸 | C. |  称量固体 | D. |  检查气密性 |
9.下列有关物质的名称、俗名、化学式中,三者皆指同一物质的是( )
| A. | 氧化钙、消石灰、CaO | B. | 氢氧化钠、烧碱、NaOH | ||
| C. | 碳酸钙、熟石灰、CaCO3 | D. | 氯化氢、盐酸、HCl |
13.下列从化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O中获取的信息中,叙述错误的是( )
| A. | 在反应前后,元素的种类没有变化 | |
| B. | 在常温下,氢气与氧气混合就可以发生反应 | |
| C. | 4 g氢气与32 g氧气完全反应,可以生成36 g水 | |
| D. | 在反应前后,氢原子和氧原子的数目都没有改变 |
14.如图为某反应的微观示意图,其中不同的球代表不同元素的原子.下列说法错误的是( )


| A. | 生成物可能都是氧化物 | |
| B. | 乙中元素的化合价在反应前后发生变化 | |
| C. | 反应前后原子的种类和数目都不变 | |
| D. | 生成物的分子个数比为1:1 |