题目内容
某兴趣小组同学对实验室制备氧气的条件进行如下探究.
实验一:为探究不同催化剂对氯酸钾分解速率的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
(1)Ⅰ中反应的化学符号表达式是________;
(2)Ⅱ中x的值应为________.
实验二:乙探究了影响双氧水(即过氧化氢溶液)分解速率的某种因素.实验数据如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
解:实验一:(1)氯酸钾在二氧化锰的催化作用下加热能快速的产生氧气,反应的化学方程式是2KClO3  2KCl+3O2↑;
2KCl+3O2↑;
故答案为:2KClO3 2KCl+3O2↑.
2KCl+3O2↑.
(2)进行实验探究时要注意控制变量,除了催化剂不同外其它应相同,故X为3.0.
故答案为:3.0.
实验二:根据表格提供的数据可以看出,双氧水的浓度越大,相同的时间产生氧气的体积越大.
故答案为:双氧水浓度越大.
分析:实验一:根据已有的知识进行分析,(1)根据氯酸钾在二氧化锰的催化作用下加热能快速的产生氧气写出化学方程式;
(2)进行实验探究时要注意控制变量;
实验二:根据表中数据进行分析.
点评:本题通过实验探究了二氧化锰和氧化铜在过氧化氢制氧气中的催化作用,侧重实验能力和分析能力的考查.
 2KCl+3O2↑;
2KCl+3O2↑;故答案为:2KClO3
 2KCl+3O2↑.
2KCl+3O2↑.(2)进行实验探究时要注意控制变量,除了催化剂不同外其它应相同,故X为3.0.
故答案为:3.0.
实验二:根据表格提供的数据可以看出,双氧水的浓度越大,相同的时间产生氧气的体积越大.
故答案为:双氧水浓度越大.
分析:实验一:根据已有的知识进行分析,(1)根据氯酸钾在二氧化锰的催化作用下加热能快速的产生氧气写出化学方程式;
(2)进行实验探究时要注意控制变量;
实验二:根据表中数据进行分析.
点评:本题通过实验探究了二氧化锰和氧化铜在过氧化氢制氧气中的催化作用,侧重实验能力和分析能力的考查.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目

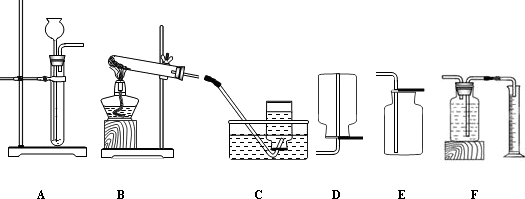

 某兴趣小组同学对实验室制备氧气的条件,及氧气的性质进行如下探究.
某兴趣小组同学对实验室制备氧气的条件,及氧气的性质进行如下探究.

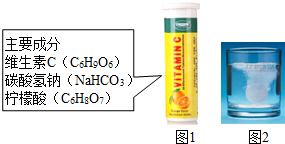 维C泡腾片(主要成分见图1)溶于水,有许多气泡产生(如图2).某兴趣小组同学对气体的成分进行如下探究.
维C泡腾片(主要成分见图1)溶于水,有许多气泡产生(如图2).某兴趣小组同学对气体的成分进行如下探究.