题目内容
 为测定空气中氧气与氮气的体积比,某同学设计了如图所示的装置进行实验.具体操作是:先关闭弹簧夹;再将螺旋状的铜丝在酒精灯上灼烧后,迅速插入大试管接触试管底部的白磷(过量);然后立即塞紧橡胶塞.他观察到大试管中产生大量的白烟.请你帮他解答下列问题:
为测定空气中氧气与氮气的体积比,某同学设计了如图所示的装置进行实验.具体操作是:先关闭弹簧夹;再将螺旋状的铜丝在酒精灯上灼烧后,迅速插入大试管接触试管底部的白磷(过量);然后立即塞紧橡胶塞.他观察到大试管中产生大量的白烟.请你帮他解答下列问题:(1)写出白磷燃烧的化学方程式
(2)待试管冷却后打开弹簧夹,此时可观察到的现象为
(3)如果装置气密性不好,测出氧气与氮气的体积比将
分析:(1)默写白磷燃烧的化学方程式;
(2)根据白磷燃烧生成白色固体五氧化二磷而使试管内气体体积减小,结合空气中氧气含量分析实验中出现的现象,并利用对压强的认识解释出现该现象的原因;
(3)分析装置气密性不好在冷却过程中可能出现的意外,判断该意外情况对实验测出氧气与氮气的体积比的影响.
(2)根据白磷燃烧生成白色固体五氧化二磷而使试管内气体体积减小,结合空气中氧气含量分析实验中出现的现象,并利用对压强的认识解释出现该现象的原因;
(3)分析装置气密性不好在冷却过程中可能出现的意外,判断该意外情况对实验测出氧气与氮气的体积比的影响.
解答:解:(1)白磷在空气中燃烧,与空气中氧气反应生成五氧化二磷,反应的化学方程式为4P+5O2
2P2O5;
(2)白磷燃烧消耗氧气,待试管冷却后,由于占空气体积
的氧气被完全反应,管内气体体积减小,使试管内压强减小的缘故,打开弹簧夹,水倒流入试管内,填补原来氧气所占体积,因此进入的水的体积约占试管容积的
;
(3)如果装置气密性不好,在进行冷却过程中,外界空气进入试管,而导致进入水的体积偏小,则测出氧气与氮气的体积比偏小;
故答案为:
(1)4P+5O2
2P2O5
(2)水倒流入试管内,约占试管容积的
;白磷燃烧消耗氧气,使试管内压强减小的缘故
(3)偏小
| ||
(2)白磷燃烧消耗氧气,待试管冷却后,由于占空气体积
| 1 |
| 5 |
| 1 |
| 5 |
(3)如果装置气密性不好,在进行冷却过程中,外界空气进入试管,而导致进入水的体积偏小,则测出氧气与氮气的体积比偏小;
故答案为:
(1)4P+5O2
| ||
(2)水倒流入试管内,约占试管容积的
| 1 |
| 5 |
(3)偏小
点评:利用可燃物耗尽空气中氧气,测量所剩余气体的体积而得到空气中氧气的体积分数,实验中要求可燃物燃烧不能产生新的气体.

练习册系列答案
相关题目
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
探究问题:红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
查阅资料:
①红磷、白磷对比情况
②镁条可以与空气中多种物质反应,如N2、CO2等
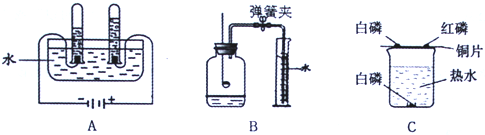
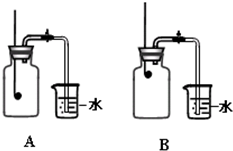
探究过程:如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
(1)红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是 .
(2)若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是 .
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式 .
探究结论:几种物质中,红磷是最适用于测定空气中氧气含量.
探究问题:红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
查阅资料:
①红磷、白磷对比情况
| 红磷 | 白磷 | |
| 状态 | 暗红色固体 | 蜡状固体 有毒 |
| 燃烧温度 | 240°C | 40°C |
探究过程:如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
(1)红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是
| 实验步骤 | 实验现象 | 结论和化学方程式 |
如图所示,将足量红磷放到燃烧匙中,点燃红磷,进行实验 |
空气中氧气约占 化学方程式 |
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式
探究结论:几种物质中,红磷是最适用于测定空气中氧气含量.
 某校化学兴趣小组就空气中氧气的含量进行实验探究:
某校化学兴趣小组就空气中氧气的含量进行实验探究: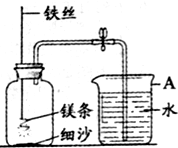 A仪器的名称是
A仪器的名称是
 (1)为测定空气中氧气的含量,某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹.用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象.
(1)为测定空气中氧气的含量,某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹.用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象.