题目内容
称取碳酸钠固体粉末21.2克置于烧杯中,慢慢加入稀盐酸使其充分反应,直至气体不再产生为止,此时共用稀盐酸221.6克,试计算:
(1)产生的二氧化碳的质量为多少?
(2)反应后所得溶液的溶质质量分数是多少?
(1)产生的二氧化碳的质量为多少?
(2)反应后所得溶液的溶质质量分数是多少?
解:设产生CO2质量为X,产生NaCl质量为Y。
Na2CO3+2HCl==2NaCl+H2O+CO2↑
106 117 44
21.2g Y X
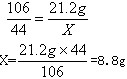
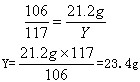
反应后所得溶液的溶质质量分数=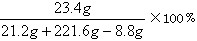 =10﹪
=10﹪
Na2CO3+2HCl==2NaCl+H2O+CO2↑
106 117 44
21.2g Y X
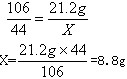
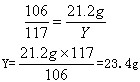
反应后所得溶液的溶质质量分数=
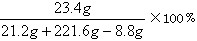 =10﹪
=10﹪
练习册系列答案
相关题目