题目内容
18.30g的某有机物和氧气恰好完全反应,只生成88g二氧化碳和54g水,则该有机物中( )| A. | 含有碳、氢、氧三种元素 | |
| B. | 只含有碳、氢两种元素 | |
| C. | 一定含有碳、氢元素,可能含有氧元素 | |
| D. | 无法确定 |
分析 根据质量守恒定律可知:生成二氧化碳中碳元素的质量等于该化合物中碳元素的质量;生成的水中氢元素的质量等于该化合物中氢元素的质量;其余则为氧元素的质量.根据该化合物的元素质量就可以确定其元素组成.
解答 解:根据碳元素和氢元素守恒可知,有机物中含碳元素为:88g×$\frac{12}{44}$×100%=24g,氢元素的质量为:54g×$\frac{2}{18}$×100%=6g,则24g+6g=30g.即该化合物是由碳元素、氢元素组成的.
故选B.
点评 物质在氧气中完全燃烧,产物只有二氧化碳和水.根据化学反应前后元素的种类和质量都不变,则生成的二氧化碳中碳元素的质量就是物质中碳元素的质量;生成的水中氢元素的质量就是物质中氢元素的质量.若碳元素与氢元素的质量和等于物质质量,则物质中不含氧元素;若小于物质质量,则物质中含有氧元素.

练习册系列答案
相关题目
10. 小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )
小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )
 小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )
小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )| 甲 | 乙 | 丙 | 丁 | |
| A | 碱 | 烧碱 | 氢氧化钾 | 纯碱 |
| B | 有机物 | 甲烷 | 蛋白质 | 淀粉 |
| C | 溶液 | 糖水 | 生理盐水 | 泥浆 |
| D | 化石燃料 | 石油 | 煤 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
7.今年4月16日,国务院发布《水污染防治行动计划》指出:2030年将消除城市臭水.下列不利于水污染防治的是( )
| A. | 多宣传不向洛阳江随意倒垃圾 | B. | 多倡导废旧电池集中回收处理 | ||
| C. | 多鼓励开办化工厂以发展经济 | D. | 多开展植树造林 |
8.小明家的水稻出现了倒伏现象,应施用的肥料是( )
| A. | CO(NH2)2 | B. | KOH | C. | Ca(H2PO4)2 | D. | KCl |
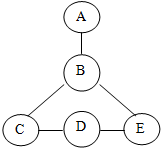 A~E均为初中化学中常见的物质,它们之间的关系如图所示,相互之间连线表示能发生化学反应.已知A和B反应时火星四射,C、D、E为不同类别的化合物,E的溶液为蓝色.回答下列问题:
A~E均为初中化学中常见的物质,它们之间的关系如图所示,相互之间连线表示能发生化学反应.已知A和B反应时火星四射,C、D、E为不同类别的化合物,E的溶液为蓝色.回答下列问题: