题目内容
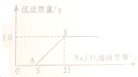 小华用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取CO2.实验完毕,他的同伴小阳决定用实验后的废液,测定桌上另一瓶Na2CO3溶液的溶质质量分数.小阳将废液过滤后,向滤液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.
小华用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取CO2.实验完毕,他的同伴小阳决定用实验后的废液,测定桌上另一瓶Na2CO3溶液的溶质质量分数.小阳将废液过滤后,向滤液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.(1)在加入Na2CO3溶液前,滤液中的溶质有
CaCl2、HCl
CaCl2、HCl
.(2)计算Na2CO3溶液中溶质的质量分数.
分析:在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明碳酸钠并没有和氯化钙反应,滤液中的溶质除含有CaCl2外,还含有盐酸,由图意,(25 g-5 g) Na2CO3溶液与氯化钙溶液全部反应,生成5 g碳酸钙沉淀,要计算碳酸钠溶液中溶质的质量分数,可根据生成沉淀的质量为5g,求出碳酸钠的质量,而这些碳酸钠是20g碳酸钠溶液中的碳酸钠的质量,就不难求出质量分数了.
解答:解:(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明碳酸钠并没有和氯化钙反应,滤液中的溶质除含有碳酸钙和盐酸反应产生的CaCl2外,还含有盐酸.(2)分析图意,(25 g-5 g) Na2CO3溶液与氯化钙溶液全部反应,生成5g碳酸钙沉淀
设:20gNa2CO3溶液中溶质的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 5g
=
x=5.3g
该Na2CO3溶液中溶质的质量分数为
×100%=26.5%
故答案为:(1)CaCl2、HCl;(2)答:Na2CO3溶液中溶质的质量分数为26.5%.
设:20gNa2CO3溶液中溶质的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 5g
| 106 |
| x |
| 100 |
| 5g |
x=5.3g
该Na2CO3溶液中溶质的质量分数为
| 5.3g |
| 25g-5g |
故答案为:(1)CaCl2、HCl;(2)答:Na2CO3溶液中溶质的质量分数为26.5%.
点评:根据反应的化学方程式能表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目

 ,需石灰石多少克?
,需石灰石多少克?