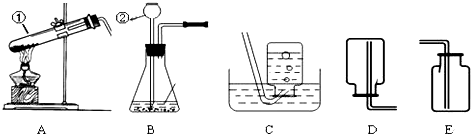
题目内容
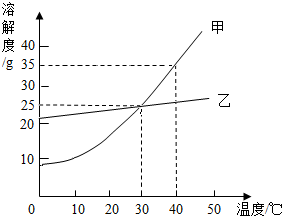 如图是甲、乙两固体物质的溶解度随温度变化的曲线图,据此我能回答下列问题:
如图是甲、乙两固体物质的溶解度随温度变化的曲线图,据此我能回答下列问题:(1)30℃时,向100g水中加入30g乙物质,充分溶解后,所得溶液是
(2)若甲物质中混有少量乙物质,若要提纯甲应采取的结晶方法是
(3)观察此曲线图,你还能获得哪些信息
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用
专题:溶液、浊液与溶解度
分析:(1)据该温度下乙的溶解度和溶质的质量分数计算分析解答;
(2)据物质的溶解度受温度影响情况分析解答;
(3)据物质的溶解度曲线可知某温度下物质的溶解度、比较同一温度下不同物质的溶解度大小,物质的溶解度受温度影响情况等.
(2)据物质的溶解度受温度影响情况分析解答;
(3)据物质的溶解度曲线可知某温度下物质的溶解度、比较同一温度下不同物质的溶解度大小,物质的溶解度受温度影响情况等.
解答:解:(1)30℃时乙的溶解度是25g,即100g水中最多溶解25g的乙,所以向100g水中加入30g乙物质,充分溶解后,还有5g不溶解,所得溶液是 饱和溶液,所得溶液中溶质的质量分数是
×100%=20%;
(2)甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以若甲物质中混有少量乙物质,若要提纯甲应采取冷却热饱和溶液的结晶方法;
(3)观察此曲线图,还可以看出30℃时甲乙两物质的溶解度相等,为25g,温度小于30℃时甲的溶解度小于乙的溶解度等;
故答案为:(1)饱和;20%; (2)冷却热饱和溶液; (3)30℃时甲乙两物质的溶解度相等,为25g(合理均可).
| 25g |
| 125g |
(2)甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以若甲物质中混有少量乙物质,若要提纯甲应采取冷却热饱和溶液的结晶方法;
(3)观察此曲线图,还可以看出30℃时甲乙两物质的溶解度相等,为25g,温度小于30℃时甲的溶解度小于乙的溶解度等;
故答案为:(1)饱和;20%; (2)冷却热饱和溶液; (3)30℃时甲乙两物质的溶解度相等,为25g(合理均可).
点评:明确溶解度曲线的意义和溶液中溶质的质量分数的计算方法是解答此题的关键因素,考查了学生对知识的掌握和应用.

练习册系列答案
相关题目
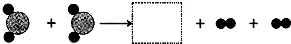 如图为某化学反应的微观过程,其中“
如图为某化学反应的微观过程,其中“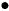 ”和“
”和“ ”表示两种不同原子.
”表示两种不同原子. B.
B. C.
C. D.
D.