题目内容
实验室用15%的氢氧化钠溶液洗涤一定量石油中残余硫酸,共消耗氢氧化钠溶液20克,洗涤后的溶液pH等于7,求这一定量的石油中含硫酸的质量是多少?
【答案】分析:溶液pH等于7即溶液呈中性说明两种溶液恰好完全反应,利用溶液的溶质质量分数计算氢氧化钠溶液中氢氧化钠质量,然后根据反应的化学方程式计算硫酸质量.
解答:解:设石油产品中含H2SO4的质量是x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
20g×15% x
=3g
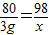
解得:x=3.675g
答:这一定量的石油中含硫酸的质量是3.675g.
点评:本道题目比较简单,是基本的根据化学方程式的计算题,关键是要看清题意,将氢氧化钠和氢氧化钠溶液的质量区分清楚.
解答:解:设石油产品中含H2SO4的质量是x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
20g×15% x
=3g
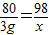
解得:x=3.675g
答:这一定量的石油中含硫酸的质量是3.675g.
点评:本道题目比较简单,是基本的根据化学方程式的计算题,关键是要看清题意,将氢氧化钠和氢氧化钠溶液的质量区分清楚.

练习册系列答案
相关题目
 15、去年6月5日世界环境日的主题为:“水--20亿人生命之所系”.请你参与下列问题的讨论.
15、去年6月5日世界环境日的主题为:“水--20亿人生命之所系”.请你参与下列问题的讨论.
 是,下列说法不正确的是
是,下列说法不正确的是 是,下列说法不正确的是
.
是,下列说法不正确的是
. 是,下列说法不正确的是______.
是,下列说法不正确的是______. 是,下列说法不正确的是______.
是,下列说法不正确的是______.