题目内容
14.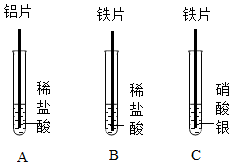 比较铝、铁、银三种金属活动性,设计如图实验:
比较铝、铁、银三种金属活动性,设计如图实验:(1)使用铝片前打磨目的是除去铝表面的氧化膜;
(2)把B试管中的稀盐酸换成氯化铝溶液,即可用B试管和C试管中的现象比较出铝、铁、银三种金属活动性;
(3)C试管中发生反应的化学方程式为Fe+2AgNO3═Fe(NO3)2+2Ag.
分析 (1)根据铝能与氧气反应分析回答;
(2)根据金属活动性顺序,验证金属的活动性顺序是否合理,可根据“反应则活泼,不反应则不活泼”进行分析判断;
(3)根据铁能与硝酸银反应写出反应的化学方程式.
解答 解:(1)由于铝能与氧气在其表面形成了一层致密的氧化膜,所以使用铝片前打磨目的是除去铝表面的氧化膜;
(2)由图示可知,把B试管中的稀盐酸换成氯化铝溶液,铁不能与氯化铝反应说明了铝的活动性大于铁,通过C试管中铁能与硝酸银反应,说明了铁的活动性大于银,即可比较出铝、铁、银三种金属活动性;
(3)C试管中铁的活动性大于银,能将银置换出来,发生反应的化学方程式为:Fe+2AgNO3═Fe(NO3)2+2Ag.
故答为:(1)除去铝表面的氧化膜;(2)氯化铝;(3)Fe+2AgNO3═Fe(NO3)2+2Ag.
点评 本题难度不大,了解金属的性质和金属活动性顺序表的应用是解答本题的基础.

练习册系列答案
相关题目
2.量筒的使用正确的是( )
| A. |  分子不断运动的实验 | B. |  取液体 | ||
| C. |  粗盐溶解 | D. | 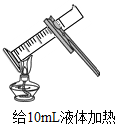 加热 |
19.下列关于碳和碳的化合物的说法,错误的是( )
| A. | 金刚石、石墨的物理性质差异很大,是因为碳原子结构不同 | |
| B. | 一氧化碳、二氧化碳化学性质不同,是因为构成它们的分子种类不同 | |
| C. | 碳、一氧化碳都能与氧化铜反应,是因为它们都具有还原性 | |
| D. | 碳酸钠、碳酸钡都能与盐酸反应生成二氧化碳,是因为它们都含有碳酸根 |
19.填表:
| 元素名称 | 氮 | 氧 | 铝 | 磷 | 钡 | 铁 | ||||
| 元素符号 | C | H | Zn | S |