题目内容
5.实验室用密度为1.84g/cm3、质量分数为98%的浓硫酸和蒸馏水,配制500g 质量分数为20%的稀硫酸.需要用多少mL的量筒量取多少mL的浓硫酸?分析 利用m=ρV、溶质质量=溶液质量×溶质的质量分数,溶液稀释前后溶质质量不变,据此结合题意进行分析解答.
解答 解:设需要98%的浓硫酸的体积为x
由溶液稀释前后溶质质量不变,
则1.84g/cm3×98%×x=500g×20%
x≈55.5cm3=55.5mL.
选取量筒时,尽量选用能一次量取的最小规格的量筒,量取55.5mL浓硫酸,应选用100mL的量筒.
故答案为:100;55.5.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、稀释前后溶质的质量不变、量筒的使用方法等是正确解答本题的关键.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案
相关题目
20.下列有关溶液的说法中正确的是( )
| A. | 均一、稳定的液体都是溶液 | |
| B. | 饱和溶液一定比不饱和溶液浓 | |
| C. | 溶液一定是液体 | |
| D. | 餐具上的油污可利用洗涤剂的乳化功能将其洗去 |
10.研究食盐可以从不同的角度进行,下列不是化学研究领域的是( )
| A. | 食盐的成分和组成 | B. | 食盐的产地 | ||
| C. | 食盐的性质和用途 | D. | 食盐的微观结构 |
17.小兴趣小组同学发现实验台上整齐摆放的药品中(见图),有一试剂瓶的标签破损.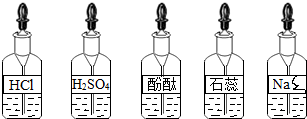
【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是酸(填物质类别);
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaHCO3溶液.
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断这是一种碱性溶液.对他的操作方法、测量结果及结论的评价,正确的是B;
A.方法正确,结果正确,且结论正确
B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确
D.方法正确,结果正确,但结论不正确
(2)小明认为它是NaOH溶液,小俊认为它是Na2CO3溶液.要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来.他们又进行了实验.
(3)小丽同学在做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生.怀疑是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了.
【进一步实验】小丽同学要用此溶液制取纯净的氢氧化钠溶液,继续完成中和反应实验.请你帮助她解决该问题:
取该氢氧化钠溶液于试管中,加入适量的氢氧化钙溶液,至溶液中不再产生沉淀为止,过滤,得到溶液即可继续使用.

【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是酸(填物质类别);
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaHCO3溶液.
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断这是一种碱性溶液.对他的操作方法、测量结果及结论的评价,正确的是B;
A.方法正确,结果正确,且结论正确
B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确
D.方法正确,结果正确,但结论不正确
(2)小明认为它是NaOH溶液,小俊认为它是Na2CO3溶液.要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来.他们又进行了实验.
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取少量样品于试管中 向其中滴入适量的稀盐酸 | 有气泡产生 | 猜想②正确 相关的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
【进一步实验】小丽同学要用此溶液制取纯净的氢氧化钠溶液,继续完成中和反应实验.请你帮助她解决该问题:
取该氢氧化钠溶液于试管中,加入适量的氢氧化钙溶液,至溶液中不再产生沉淀为止,过滤,得到溶液即可继续使用.
 甲、乙两种固体物质的溶解度曲线如图所示,现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯中,再向烧杯中加入一定量的浓硫酸.
甲、乙两种固体物质的溶解度曲线如图所示,现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯中,再向烧杯中加入一定量的浓硫酸.