题目内容
13. 实验室常用锌粒和稀硫酸反应制取氢气,如图
实验室常用锌粒和稀硫酸反应制取氢气,如图①反应的方程式:Zn+H2SO4═ZnSO4+H2↑
②选用F作为制取氢气的发生装置的优点是可以随时控制反应的发生和停止.
③G装置若用于排空气法收集氢气,氢气应从b端通入.若瓶中先装满水,用排水法收集氢气时,氢气应从b端通入.(选填“a”或“b”)
分析 ①锌粒和稀硫酸反应制取氢气,同时生成硫酸锌,进行分析解答.
②F装置课通过关闭和打开,控制液体与固体的接触,进行分析解答.
③用排水法收集氢气时,长导管是出水管,进行分析解答.
解答 解:①锌粒和稀硫酸反应制取氢气,同时生成硫酸锌,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
②关闭F装置中的弹簧夹后,装置内产生的气体排不出去,装置内的气体压强增大,使液体被压回长颈漏斗,液面下降,反应液与块状固体脱离,反应停止;使反应发生,打开弹簧夹即可;所以F作为氢气发生装置的优点是可以随时控制反应的发生和停止.
③若瓶中先装满水,用排水法收集氢气时,长导管是出水管,氢气应从b端通入.
故答案为:①Zn+H2SO4═ZnSO4+H2↑;②可以随时控制反应的发生和停止;③b.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取氢气的反应原理、收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
相关题目
8.煤气中添加少量有特殊臭味的乙硫醇(C2H5SH)可提示煤气是否泄漏.乙硫醇在煤气燃烧过程中也可充分燃烧,化学方程式为2C2H5SH+9O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2X+6H2O.下列叙述不正确的是( )
| A. | X为SO2 | B. | 乙硫醇的相对分子质量为62g | ||
| C. | 乙硫醇由三种元素组成 | D. | 乙硫醇燃烧不充分时也可产生CO |
2.5月31日是“世界无烟日”.吸烟对人体有害,吸烟产生的气体中含有一种能与血液中血红蛋白结合的有毒气体,它是( )
| A. | CO2 | B. | SO2 | C. | CO | D. | H2O |

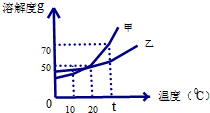 观察图甲、乙两种物质的溶解度曲线回答问题
观察图甲、乙两种物质的溶解度曲线回答问题 用化学方程式表示下列物质间的转化
用化学方程式表示下列物质间的转化