题目内容
2.已知金属R于硫酸铜溶液反应的化学方程式为:R+CuSO4=Cu+RSO4则下列说法正确的是( )| A. | RSO4中R的化合价无法得出 | B. | 金属R的活动性比铜强 | ||
| C. | 该金属一定是铝 | D. | 该金属一定是铁 |
分析 根据题意,R+CuSO4=Cu+RSO4,说明R的金属活动性比铜强;由生成的RSO4,硫酸根显-2价,则R元素显+2价,据此进行分析判断.
解答 解:A、RSO4中硫酸根显-2价,则R元素显+2价,故选项说法错误.
B、由R+CuSO4=Cu+RSO4,说明R的金属活动性比铜强,故选项说法正确.
C、R元素显+2价,铝显+3价,该金属不可能是铝,故选项说法错误.
D、R元素显+2价,且R的金属活动性比铜强,R可能是铁,也可能是锌等其它金属,故选项说法错误.
故选:B.
点评 本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.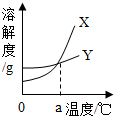 已知氯化钠和硝酸钾的溶解度表与溶解度曲线图如图:
已知氯化钠和硝酸钾的溶解度表与溶解度曲线图如图:
下列有关说法正确的是( )
 已知氯化钠和硝酸钾的溶解度表与溶解度曲线图如图:
已知氯化钠和硝酸钾的溶解度表与溶解度曲线图如图:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
| A. | X是氯化钠的溶解度曲线 | |
| B. | 溶解度曲线图上的温度a介于10℃~30℃之间 | |
| C. | 60℃时,100g水中加入100g硝酸钾,充分溶解,所得溶液是饱和溶液 | |
| D. | 从硝酸钾和氯化钠(少量)的混合物中分离出硝酸钾常采用蒸发结晶法 |
17.经过一段时间的化学学习,你认为不属于化学这门科学研究范畴的是( )
| A. | 物质的运动状态 | B. | 物质的变化和性质 | ||
| C. | 物质的组成和结构 | D. | 物质的制取和用途 |
14.下列物质的化学式、俗名和类别全部正确的是( )
| A. | CaO生石灰碱 | B. | Na2CO3纯 碱 碱 | ||
| C. | C2H5OH 酒精 氧化物 | D. | NaHCO3小苏打盐 |
11. 行车是一种绿色出行工具.
行车是一种绿色出行工具.
(1)如图所示的自行车车体所用的材料中,属于有机合成材料的是BD.
(2)炎热的夏季自行车要放在阴凉处,否则容易爆胎,爆胎原因的微观解释是温度升高,气体分子间距离加大,分子运动速率加快,胎内压强增大.
(3)碳素钢是常用的车架材料,容易生锈,其生锈的条件是与氧气和水同时接触.
(4)碳纤维是一种含碳量在95%以上的高强度新型纤维材料,其中含碳量高于99%的称为石墨纤维.碳纤维“外柔内刚”,质量比金属铝轻,但强度却高于钢铁,并且具有耐腐蚀性.碳纤维车架材料用碳纤维、树脂、玻璃纤维、铝合金复合而成,是目前质量最轻的车架材料.下列说法不正确的是C.
 行车是一种绿色出行工具.
行车是一种绿色出行工具.(1)如图所示的自行车车体所用的材料中,属于有机合成材料的是BD.
(2)炎热的夏季自行车要放在阴凉处,否则容易爆胎,爆胎原因的微观解释是温度升高,气体分子间距离加大,分子运动速率加快,胎内压强增大.
(3)碳素钢是常用的车架材料,容易生锈,其生锈的条件是与氧气和水同时接触.
(4)碳纤维是一种含碳量在95%以上的高强度新型纤维材料,其中含碳量高于99%的称为石墨纤维.碳纤维“外柔内刚”,质量比金属铝轻,但强度却高于钢铁,并且具有耐腐蚀性.碳纤维车架材料用碳纤维、树脂、玻璃纤维、铝合金复合而成,是目前质量最轻的车架材料.下列说法不正确的是C.
| A.碳纤维具有可燃性 | B.碳纤维车架耐腐蚀 |
| C.碳纤维车架材料遇酸不反应 | D.碳纤维的密度小 |