题目内容
某校研究性学习小组得到一块铁制品,不知它是生铁还是钢,几位同学设计了一个实验来进行鉴定.他们用200ml稀盐酸(密度为1.04g/cm3)分四次加入到金属块上,生成的氢气能被完全收集起来进行称量,实验数据记录在下表(此块制品假设只是由铁和单质碳两种物质组成的,碳不与盐酸反应也不溶于盐酸).生铁含碳质量分数为2%~4.3%.)| 次数 | 加入盐酸的量 | 生成H2的总质量 | 剩余固体质量 |
| 1 | 50ml | 0.2g | |
| 2 | 50ml | 0.4g | |
| 3 | 50ml | 0.6g | 0.2g |
| 4 | 50ml | 0.6g | 0.2g |
(1)第______次加入盐酸并充分反应后,制品中的铁和盐酸恰好完全反应.
(2)通过计算回答:这块铁制品中单质碳的质量分数为多少?它是生铁还是钢?
(3)求所用的盐酸溶液中HCl的质量分数?
【答案】分析:由实验数据记录表,每50mL稀盐酸完全反应可生成0.2gH2;金属制品完全反应生成0.6gH2;由于第四次加入50mL稀盐酸,产生H2质量与不再增加,说明前三次所加入的150mL稀盐酸已把金属制品中的铁完全反应.
解答:解:(1)根据前三次加入稀盐酸与生成H2的关系,当加入150mL稀盐酸,金属制品中铁恰好与稀盐酸完全反应;
故答:3;
(2)设制品中Fe的质量为x,三次参加反应的HCl质量为y
依据题意得:Fe+2HCl=FeCl2+H2↑
56 73 2
x y 0.6g
56:2=x:0.6g
73:2=y:0.6g
解之得:x=16.8g y=21.9g
铁制品中单质碳的质量分数=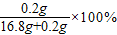 ≈1.18%
≈1.18%
∵1.18%<2%,∴铁制品属于钢
答:这块铁制品中单质碳的质量分数为1.18%,它是钢;
(3)盐酸溶液中HCl的质量分数=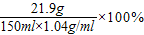 ≈14.04%
≈14.04%
答:所用的盐酸溶液中HCl的质量分数为14.04%.
点评:由第四次加入50mL稀盐酸氢气质量不再增加、剩余固体质量不再减少,可得知第四次加入的稀盐酸因铁在前三次已被完全反应而未发生反应.
解答:解:(1)根据前三次加入稀盐酸与生成H2的关系,当加入150mL稀盐酸,金属制品中铁恰好与稀盐酸完全反应;
故答:3;
(2)设制品中Fe的质量为x,三次参加反应的HCl质量为y
依据题意得:Fe+2HCl=FeCl2+H2↑
56 73 2
x y 0.6g
56:2=x:0.6g
73:2=y:0.6g
解之得:x=16.8g y=21.9g
铁制品中单质碳的质量分数=
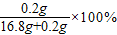 ≈1.18%
≈1.18%∵1.18%<2%,∴铁制品属于钢
答:这块铁制品中单质碳的质量分数为1.18%,它是钢;
(3)盐酸溶液中HCl的质量分数=
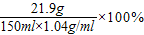 ≈14.04%
≈14.04%答:所用的盐酸溶液中HCl的质量分数为14.04%.
点评:由第四次加入50mL稀盐酸氢气质量不再增加、剩余固体质量不再减少,可得知第四次加入的稀盐酸因铁在前三次已被完全反应而未发生反应.

练习册系列答案
相关题目
(1)某校研究性学习小组欲配制1000g溶质质量分数为15%的氢氧化钠溶液.需氢氧化钠固体 g,水 mL(水的密度是1g/cm3);称量氢氧化钠时 (填“能”或“不能”)放在纸上称量.
(2)甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关.
【理论分析】:
①甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是 .
②乙同学的猜想也不正确,理由是 .
【实验设计】:
③为证实丙同学的猜想,还需作如下实验,请完成下表.
④通过以上实验,四位同学看到:溶液先变成红色,一会儿红色又消失.因此酚酞红色褪去与氧气无关.若丁同学的猜想正确,设计如下实验证明并完成有关问题:
实验方法:观察到的现象和结论;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明
.
方案二:将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释观察到的现象和结论: .
(4)(8分)该校研究性学习小组向上述所配制的15%的氢氧化钠溶液中滴加稀盐酸,有气泡产生,由此可知所用的NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式 ;所以氢氧化钠应该 保存.(2分)
【提出问题】:所用的NaOH变质程度怎样?
【设计方案】:先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数.
【进行实验】:实验测得加入稀硫酸的质量与产生CO2气体的质量关系如下图所示.
【数据处理】:写出以下计算过程:
(5)该样品中NaOH的质量分数为多少?
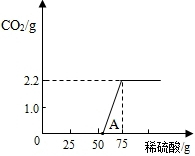
【反思与交流】:①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入稀硫酸,首先反应的物质是 ;②根据反应方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗稀硫酸的量 (填“相等”或“大于”或“小于”.(2分)
(2)甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关.
【理论分析】:
①甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是
②乙同学的猜想也不正确,理由是
【实验设计】:
③为证实丙同学的猜想,还需作如下实验,请完成下表.
| 实验步骤 | 设计这一步骤的目的 |
| 1.用煮沸过的蒸馏水配制氢氧化钠溶液. | |
| 2.在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油. |
实验方法:观察到的现象和结论;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明
方案二:将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释观察到的现象和结论:
(4)(8分)该校研究性学习小组向上述所配制的15%的氢氧化钠溶液中滴加稀盐酸,有气泡产生,由此可知所用的NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式
【提出问题】:所用的NaOH变质程度怎样?
【设计方案】:先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数.
【进行实验】:实验测得加入稀硫酸的质量与产生CO2气体的质量关系如下图所示.
【数据处理】:写出以下计算过程:
(5)该样品中NaOH的质量分数为多少?

【反思与交流】:①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入稀硫酸,首先反应的物质是

 (2010?雅安)某校研究性学习小组进行了一个有趣的实验探究:
(2010?雅安)某校研究性学习小组进行了一个有趣的实验探究: 类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:
类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究: