题目内容
14.某实验小组在实验室用加热氯酸钾和二氧化锰的混合物来制取氧气,反应一段时间收集到所需的氧气后停止加热,老师鼓励他们对剩余固体的成分进行探究,于是小组成员对其成分进行如下猜想:甲认为是:KClO3、KCl、MnO2 乙认为是KCl、MnO2 丙认为是:KClO3、MnO2
(1)请你根据所学知识判断丙的猜想一定是错误的;理由是KCl为生成物,反应后一定存在.
(2)请帮助甲同学验证自己的猜想:取适量的剩余固体加入到试管中加热,然后用带火星的木条检验,若观察到木条复燃的现象,说明甲 的猜想是正确的.
(3)通过该探究,我们得出结论,在反应一段时间后,试管中一定存在的物质是BC(不定项选择)
A、反应物 B、生成物 C、催化剂
(4)在对试管加热过程中,固体混合物中二氧化锰的质量分数将A
A、变大 B、变小 C、不变 D、无法确定.
分析 (1)根据质量守恒定律,考虑“反应一段时间收集到所需的氧气后停止加热”,进行分析;
(2)考虑氯酸钾受热会产生氧气进行分析;
(3)根据化学反应的过程以及催化剂的概念来分析;
(4)催化剂的质量不变,固体的质量减少.
解答 解:(1)因为反应一段时间了,而剩余固体中不可能无氯化钾,故“丙认为是:KClO3、MnO2”的猜想错误;
(2)为了帮助甲同学验证其的猜想:取适量的剩余固体加入到试管中加热,将带火星的木条放在试管内,若木条复燃,说明甲的猜想是正确的.
(3)在反应一段时间后,试管中一定存在的物质是生成物、催化剂,反应物可能有,也可能没有;
(4)二氧化锰作为催化剂,质量不变,而氯酸钾分解,剩余固体的质量不断减少一直到完全反应,所以在对试管加热过程中,固体混合物中二氧化锰的质量分数变大.
故答案为:
(1)丙;KCl为生成物,反应后一定存在;
(2)带火星的木条;木条复燃;甲;
(3)BC;
(4)A.
点评 本考点主要考查质量守恒定律等知识.本考点是中考的重要考点之一,主要出现在填空题中.

练习册系列答案
相关题目
2.由Na2S和Na2SO3两种物质组成的混合物中,已知硫元素的质量分数为32%,则混合物中氧元素的质量分数为( )
| A. | 22% | B. | 48% | C. | 16% | D. | 28% |
19.如表是某同学用两种方法区分不同物质的情况,其中有错误的是( )
| 选项 | 需鉴别物质 | 方法1 | 方法2 |
| A | 厕所清洁剂与炉具清洁剂 | 加入鸡蛋壳 | 加入石蕊试液 |
| B | 硬水与蒸馏水 | 加入肥皂水 | 蒸干 |
| C | 氢氧化钠溶液和石灰水 | 通入二氧化碳 | 放置于空气中看是否潮解 |
| D | 24k黄金和18k黄金 | 空气中灼烧 | 加入硝酸银溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.50mL酒精和50mL水混合后总体积小于100mL的微观原因是( )
| A. | 分子之间有间隔 | B. | 分子体积很小 | ||
| C. | 分子在不断运动 | D. | 不同物质的分子性质不同 |
3.生活中的加碘盐,补铁口服液,补锌口服液的“碘、铁、锌”指的是( )
| A. | 单质 | B. | 分子 | C. | 原子 | D. | 元素 |
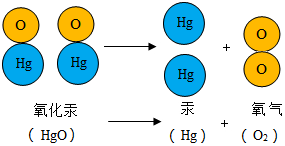 氧化汞受热时的变化可用如图表示,图中大圆圈表示汞原子,小圆圈表示氧原子,据图得出的结论中不正确的是A
氧化汞受热时的变化可用如图表示,图中大圆圈表示汞原子,小圆圈表示氧原子,据图得出的结论中不正确的是A