题目内容
9.若锌和镁混合物的质量为4.8g与100g稀硫酸恰好完全反应,则该稀硫酸的溶质质量分数可能是( )| A. | 5% | B. | 10% | C. | 15% | D. | 20% |
分析 锌和稀硫酸反应生成硫酸锌和氢气,镁和稀硫酸反应生成硫酸镁和氢气,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:设4.8g固体都是锌或镁时消耗硫酸的质量分别为x、y,
Zn+H2SO4═ZnSO4+H2↑,Mg+H2SO4═MgSO4+H2↑,
65 98 24 98
4.8g x 4.8g y
$\frac{65}{4.8g}$=$\frac{98}{x}$,$\frac{24}{4.8g}$=$\frac{98}{y}$,
x=7.2g,y=19.6g,
则硫酸的质量分数分别为:$\frac{7.2g}{100g}$×100%=7.2%,$\frac{19.6g}{100g}$×100%=19.6%,
因此稀硫酸的质量分数应该是大于7.2%,小于19.6%,
故选:BC.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
20.甲同学在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2与二氧化碳相似,能与氢氧化钠反应.
(3)点燃充满氢气的小试管,会有轻微的爆鸣声.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
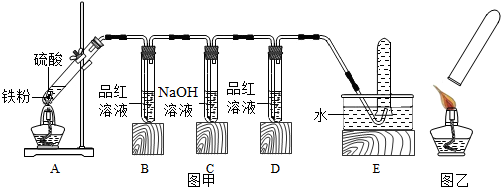
请帮助小明完成如表:
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫.
【反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】实验结束后甲同学先撤去了酒精灯,请你预测会发生什么后果引起倒吸现象,B中液体会倒吸入A,A处热试管有可能炸裂.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2与二氧化碳相似,能与氢氧化钠反应.
(3)点燃充满氢气的小试管,会有轻微的爆鸣声.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助小明完成如表:
| A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品 红溶液 | D中品 红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 不褪色 | 无爆鸣声 | 只有SO2 | |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | SO2、H2都有 |
| 实验三 | 25% | 不褪色 | 只有H2 | ||
【反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】实验结束后甲同学先撤去了酒精灯,请你预测会发生什么后果引起倒吸现象,B中液体会倒吸入A,A处热试管有可能炸裂.
17.如图为甲乙两物质的溶解度曲线,下列说法正确的是( )


| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15% | |
| C. | 将甲溶液从t2℃时降温到t1℃时,一定有晶体析出 | |
| D. | 要使接近饱和的甲溶液转化为饱和溶液,可以采用降温的方法 |
14.如图所示有关的图示和图标中正确的是( )
| A. |  浓硫酸的稀释 | B. |  实验室制取CO2 | C. |  当心火灾 | D. |  禁止吸烟 |
1.下列化学方程式符合题意且书写正确的是( )
| A. | 医疗上用碱性物质中和胃酸过多:NaOH+HCl═NaCl+H2O | |
| B. | 证明铜的活动性比银强:Cu+2AgCl═CuCl2+2Ag | |
| C. | 实验室制取氧气:2KClO3═2KCl+3O2↑ | |
| D. | 工业上用纯碱制烧碱:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
14.金属M和AgNO3溶液反应的化学方程式为:M+2AgNO3═M(NO3)2+2Ag.则下列说法错误的是( )
| A. | 这个反应属于置换反应 | |
| B. | 金属M可能是铜 | |
| C. | 用M可以回收硝酸银废液中的银 | |
| D. | 反应前后元素M和N化合价发生了变化 |
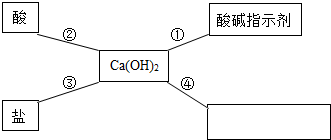 对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应.
对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应. 是某些非金属氧化物.
是某些非金属氧化物.