题目内容
9.四氯化硅(SiCl4)是一种重要的化工原料,遇水会发生如下反应:SiCl4+3H2O═H2SiO3↓+4HCl某地曾发生将含有四氯化硅的废料倒入池塘造成污染事件,事后环保人员在受污染的池塘中投放熟石灰[Ca(OH)2]做了有效处理
(1)已知H4SiO4不跟[Ca(OH)2]反应,为了确定投入熟石灰的质量,要先测定废料倒入池塘后生成HCl的质量,选用下列哪组数据能确定池塘中生成HCl的质量A.
A.倒入废料的总质量,废料中SiCl4的质量分数
B.池塘水的pH
C.池塘水中HCl的质量分数
(2)经测定池塘水中共有0.365吨HCl,则需要加入多少吨熟石灰才能将其完全反应.(列式计算,相对原子质量H:1 O:16 Cl:35.5 Ca:40)
分析 (1)根据只要知道倒入废料的总质量,废料中SiCl4的质量分数,结合化学方程式计算出生成氯化氢的质量;
(2)根据盐酸和氢氧化钙反应生成氯化钙和水,结合题中的数据进行计算.
解答 解:(1)通过分析可知,只要知道倒入废料的总质量,废料中SiCl4的质量分数,通过SiCl4+3H2O═H2SiO3↓+4HCl,即可计算生成氯化氢的质量,故选:A;
(2)设需要熟石灰为x,
Ca(OH)2+2HCl=CaCl2+2H2O
74 73
x 0.365t
$\frac{74}{x}$=$\frac{73}{0.365t}$
x=0.37t
故答案为:(1)A;(2)0.37t.
点评 本题主要考查了化学方程式的计算,难度不大,只要认真分析题意即可解答.

练习册系列答案
相关题目
19.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
Ⅰ、写出该中和反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O.
Ⅱ、探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl
【查阅资料】氯化钙溶液呈中性.
【进行实验】
【反思与拓展】
( 1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是溶液呈酸性,腐蚀管道或造成水污染.要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的石灰石.
Ⅰ、写出该中和反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O.
Ⅱ、探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl
【查阅资料】氯化钙溶液呈中性.
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡 | 溶液无明显变化或溶液不变红色 | 猜想一不正确 |
| 另取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量 | 先有气体产生,后产生沉淀 | 猜想二不正确 猜想三正确 |
( 1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是溶液呈酸性,腐蚀管道或造成水污染.要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的石灰石.
4.Na2CO3的水溶液呈碱性,下列说法错误的是( )
| A. | 碳酸钠在水中会电离出OH- | |
| B. | 往碳酸钠溶液中加稀硫酸后溶液的pH降低 | |
| C. | 碳酸钠溶液中存在OH- | |
| D. | 往碳酸钠溶液中滴加紫色石蕊试液后溶液显蓝色 |
1.下列物质分别加入适量水中,充分搅拌,能够得到溶液的是( )
| A. | 面粉 | B. | 豆油 | C. | 牛奶 | D. | 白糖 |
18. 把盛有5g 16%的NaOH溶液的短试管放入盛有10g 16%的CuSO4溶液的锥形瓶里,如图所示,倾斜锥形瓶直到使两溶液充分混合,混合后不可能的是( )
把盛有5g 16%的NaOH溶液的短试管放入盛有10g 16%的CuSO4溶液的锥形瓶里,如图所示,倾斜锥形瓶直到使两溶液充分混合,混合后不可能的是( )
 把盛有5g 16%的NaOH溶液的短试管放入盛有10g 16%的CuSO4溶液的锥形瓶里,如图所示,倾斜锥形瓶直到使两溶液充分混合,混合后不可能的是( )
把盛有5g 16%的NaOH溶液的短试管放入盛有10g 16%的CuSO4溶液的锥形瓶里,如图所示,倾斜锥形瓶直到使两溶液充分混合,混合后不可能的是( )| A. | 产生蓝色沉淀0.98g | |
| B. | 锥形瓶内物质总质量不变 | |
| C. | 所得溶液的Na2SO4质量分数大于9.5% | |
| D. | 所得的Na2SO4溶液质量与原CuSO4溶液质量相等 |
19.下列说法中不正确的是( )
| A. | 农业上可采用喷灌、滴灌来节水 | B. | 用肥皂水可区分硬水和软水 | ||
| C. | 有颜色的植物均可制成酸碱指示剂 | D. | 在钢铁表面涂油可防止生锈 |
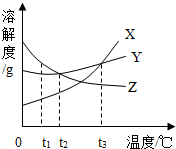 如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.
如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.