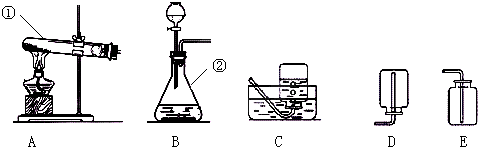
题目内容
下列实验操作中,能达到实验目的是( )| 选项 | 实验目的 | 实验操作 |
| A | 将硬水转化成软水 | 向硬水中加入絮凝剂,过滤 |
| B | 除去CaO中的CaCO3 | 加入足量的水,充分溶解,过滤 |
| C | 证明可燃物燃烧需要氧气 | 向80℃热水中的白磷通氧气 |
| D | 除去稀盐酸中混有的少量BaCl2溶液 | 加入适量的CuSO4溶液,过滤 |
A.A
B.B
C.C
D.D
【答案】分析:A、根据硬水和软水的转化方法进行分析判断.
B、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
C、根据燃烧的条件进行分析判断.
D、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:A、向硬水中加入絮凝剂、过滤,不能除去可溶性的钙镁化合物,不能将硬水转化成软水,故该实验操作不能达到实验目的.
B、CaO能与水反应生成氢氧化钙,碳酸钙不溶于水,反而会把原物质除去,不符合除杂原则,故该实验操作不能达到实验目的.
C、向80℃热水中的白磷通氧气,热水中的白磷燃烧,说明可燃物燃烧需要氧气,故该实验操作能达到实验目的.
D、适量的CuSO4溶液会和BaCl2溶液反应生成硫酸钡沉淀和氯化铜,能除去杂质但引入了新的杂质氯化铜,不符合除杂原则,故该实验操作不能达到实验目的.
故选C.
点评:本题难度不大,掌握硬水与软水的转化、抓住除杂质的原理、燃烧的条件等并能灵活运用是正确解题的关键.
B、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
C、根据燃烧的条件进行分析判断.
D、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:A、向硬水中加入絮凝剂、过滤,不能除去可溶性的钙镁化合物,不能将硬水转化成软水,故该实验操作不能达到实验目的.
B、CaO能与水反应生成氢氧化钙,碳酸钙不溶于水,反而会把原物质除去,不符合除杂原则,故该实验操作不能达到实验目的.
C、向80℃热水中的白磷通氧气,热水中的白磷燃烧,说明可燃物燃烧需要氧气,故该实验操作能达到实验目的.
D、适量的CuSO4溶液会和BaCl2溶液反应生成硫酸钡沉淀和氯化铜,能除去杂质但引入了新的杂质氯化铜,不符合除杂原则,故该实验操作不能达到实验目的.
故选C.
点评:本题难度不大,掌握硬水与软水的转化、抓住除杂质的原理、燃烧的条件等并能灵活运用是正确解题的关键.

练习册系列答案
相关题目
(2010?达州)纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证.请你帮助她将下列实验报告填写完整.
[交流与反思]若用稀硫酸代替稀盐酸进行实验,是否与猜想二相同?______(填“是”或“否”).
| 猜想 | 实验操作 | 实验现象 | 结论(或化学方程式) |
| 猜想一:Na2CO3溶液显碱性 | 取少量的Na2CO3溶液试管中,滴入2-3滴酚酞试液,振荡 | ______ | 溶液显碱性 |
| 猜想二:能与酸反应 | 取少量的Na2CO3溶液试管中,然后滴加稀盐酸 | 有大量的气泡 | 化学方程式:______ |
| 猜想三:能与Ca(OH)2反应 | 向盛有少量Na2CO3溶液的试管中滴加澄清石灰水 | 出现白色沉淀 | 化学方程式:______ |
| 猜想四:能与氯化钡反应 | ______ | 出现白色沉淀 | Na2CO3+BaCl2=BaCO3↓+2NaCl 反应的基本类型为:______ |