题目内容
18.利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如图所示(反应条件已略去):
已知:2Cu+2H2SO4+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O
(1)过程Ⅱ中分离操作的名称是过滤
(2)物质B是锌粒;若过程Ⅱ中没有气泡产生,溶液A的溶质是硫酸铜和硫酸锌
(3)过程Ⅲ中有气体产生,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
分析 根据转化流程可知,含Cu、Zn铜帽与稀硫酸和氧气反应生成了硫酸铜和硫酸锌的混合液A,依据实验的目的,为了得到铜和硫酸锌,应向A溶液加入过量的锌,通过过滤得到了硫酸锌溶液和铜锌的固体混合物C,为了得到铜和硫酸锌,应加入稀硫酸,然后结合题中的问题进行分析.
解答 解:通过分析转化流程可知,含Cu、Zn铜帽与稀硫酸和氧气反应生成了硫酸铜和硫酸锌的混合液A,依据实验的目的,为了得到铜和硫酸锌,应向A溶液加入过量的锌,通过过滤得到了硫酸锌溶液和铜锌的固体混合物C,为了得到铜和硫酸锌,应加入稀硫酸,所以
①过滤的方法可以将固体和液体分离,过程Ⅱ中为了分离固体和液体,所以操作的名称是:过滤;
②过程Ⅱ的反应是锌与硫酸铜反应生成硫酸锌和铜,过程Ⅱ中加入的物质B为金属锌;若过程Ⅱ中没有气泡产生,说明溶液A中没有硫酸剩余,溶质是硫酸铜和硫酸锌;
③过程Ⅲ中是稀硫酸与锌反应生成了硫酸锌和氢气,反应的方程式是:Zn+H2SO4=ZnSO4+H2↑;
故答案为:①过滤;
②锌粒;硫酸铜和硫酸锌;
③Zn+H2SO4=ZnSO4+H2↑.
点评 在解此类题时,要熟记和理解金属的性质及用途、常见金属的特性及其应用等相关知识,然后结合题中的问题进行分析解答.

练习册系列答案
相关题目
6.下列物质的用途与其化学性质无关的是( )
| A. | 用盐酸除铁锈 | B. | 工业上用一氧化碳炼铁 | ||
| C. | 用干冰进行人工降雨 | D. | 用碳酸氢钠的发酵粉配制糕点 |
13.下列所示是李明同学探究蜡烛燃烧火焰和蜡烛燃烧产物的实验报告,请结合课本内容补充完整.
| 实验操作步骤 | 实验现象 | 分析、结论 |
| 将一根火柴平放入蜡烛火焰中,约2s后取出 | 火柴处于蜡烛火焰外焰的地方最先炭化 | |
| 将一个冷而干燥的烧杯罩在蜡烛火焰的正上方 | ||
| 将一个内壁沾有澄清石灰水的烧杯倒扣在火焰上方 |
10.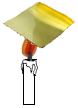 某兴趣小组同学将一块薄铜片盖在蜡烛火焰上方(如图),一段时间后,发现铜片被“熏黑”了.针对铜片上产生的黑色固体,请你参与探究.
某兴趣小组同学将一块薄铜片盖在蜡烛火焰上方(如图),一段时间后,发现铜片被“熏黑”了.针对铜片上产生的黑色固体,请你参与探究.
【查阅资料】蜡烛主要是由含C、H的有机物组成的混合物.
【猜想】同学们对黑色固体的成分作出以下猜想:
甲的猜想:黑色固体是炭黑
乙的猜想:黑色固体是氧化铜
你的猜想:黑色固体是炭黑和氧化铜
【分析】甲的猜想依据是:质量守恒定律
【实验】请设计实验,证明你的猜想是成立的,完成下表:
 某兴趣小组同学将一块薄铜片盖在蜡烛火焰上方(如图),一段时间后,发现铜片被“熏黑”了.针对铜片上产生的黑色固体,请你参与探究.
某兴趣小组同学将一块薄铜片盖在蜡烛火焰上方(如图),一段时间后,发现铜片被“熏黑”了.针对铜片上产生的黑色固体,请你参与探究.【查阅资料】蜡烛主要是由含C、H的有机物组成的混合物.
【猜想】同学们对黑色固体的成分作出以下猜想:
甲的猜想:黑色固体是炭黑
乙的猜想:黑色固体是氧化铜
你的猜想:黑色固体是炭黑和氧化铜
【分析】甲的猜想依据是:质量守恒定律
【实验】请设计实验,证明你的猜想是成立的,完成下表:
| 实验操作 | 实验现象 | 结论 |
| 将铜片上的黑色固体刮下少量至试管中,再加入过量的稀硫酸 | 溶液由无色变成蓝色,试管底部还有少量的黑色固体. | 猜想成立 |
8.关于H2的说法,正确的是( )
| A. | 氢气是密度最小的气体 | |
| B. | 点燃不纯的氢气,肯定会发生爆炸 | |
| C. | 验纯时,若听到尖锐的爆鸣声,证明氢气不纯,应立即再次收集 | |
| D. | 可以用电解水的方法来制造氢气供人们大量使用 |

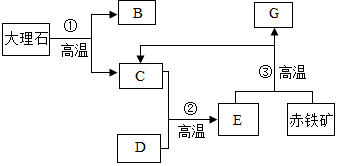 工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如图所示,已知D、G为单质.
工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如图所示,已知D、G为单质.