题目内容
请按要求完成下列金属性质的实验:
研究一:金属与酸反应过程中的能量变化.
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应 (填“吸热”或“放热”),反应的化学方程式为 .
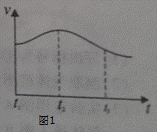
(2)实验测得反应中产生的气体的速率(v)与时间(t)的关系如图1,请根据t1﹣t2时间段反应速率变化,说明化学反应速率受 等因素影响.
研究二:金属与盐溶液反应过程中的相关变化.
(1)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为 .
(2)在一定量AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,图2描述相关变化曲线,一定不正确的是 .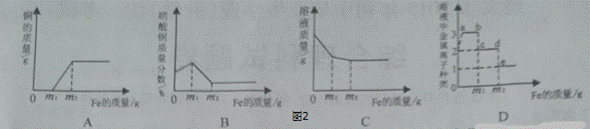
考点:
金属的化学性质;物质发生化学变化时的能量变化;书写化学方程式、文字表达式、电离方程式.
专题:
金属与金属材料.
分析:
研究一:(1)根据反应时温度的变化分析反应时能量的问题,镁与盐酸反应会生成氢气和氯化镁进行分析;
(2)根据图中反应速率的变化进行分析;
研究二:(1)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(2)根据金属活动性顺序可知,铁会先于硝酸银反应生成硝酸亚铁和银,然后再与硝酸铜反应生成硝酸亚铁和铜进行分析.
解答:
解:研究一:(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应放热,镁与盐酸反应会生成氢气和氯化镁,化学方程式为:Mg+2HCl=MgCl2+H2↑;
(2)通过图中的反应速率可以看出,在t1﹣t2时间段速率加快,所以化学反应速率受温度等因素影响;
研究二:(1)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:CuSO4+Fe=FeSO4+Cu;
(2)由金属活动性顺序可知,铁会先于硝酸银反应生成硝酸亚铁和银,然后再与硝酸铜反应生成硝酸亚铁和铜,所以
A、刚开始铜的质量为零,置换完银才会置换出铜,故A正确;
B、硝酸铜的质量分数最后会减小到零,故B错误;
C、铁和硝酸银反应生成硝酸亚铁和银,每56份质量的铁会置换出216份质量的银,溶液质量减轻,铁和硝酸铜反应生成硝酸亚铁和铜,每56份质量的铁会置换出64份质量的铜,溶液质量也会减轻,但是没有前面减小的幅度大,故C正确;
D、铁刚与硝酸银反应生成硝酸亚铁和银,溶液中会出现银离子、亚铁离子、铜离子三种离子,然后会出现亚铁离子和铜离子,然后只剩下亚铁离子,故D正确.
故选:B.
故答案为:研究一:(1)放热,Mg+2HCl=MgCl2+H2↑;
(2)温度;
研究二:(1)CuSO4+Fe=FeSO4+Cu;
(2)B.
点评:
本题难度不大,要找准题中考查的知识点即可解答.

a、b、c三种酸分别与足量的金属Mg充分反应,生成等质量的H2,反应消耗a、b、c的分子数目之比为3:6:2.下列关于a、b、c的推理合理的是(HX、H2Y、H3Z分别表示三种酸)( )
|
| A. | a、b、c三种酸溶液中的H原子数目:c>a>b |
|
| B. | a、b、c与金属Mg反应的速率:b>a>c |
|
| C. | a、b、c的相对分子质量:b<a<c |
|
| D. | a、b、c可能分别为H2Y、HX、H3Z |
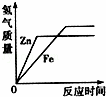
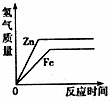
向等质量的锌粉和铁粉中分别加入足量稀硫酸,下列图象描述正确的是( )
|
| A. |
| B. |
| C. |
| D. |
|
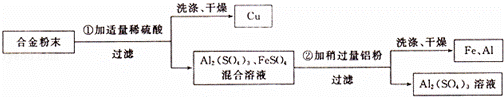
用廉价金属回收贵重金属是工业生产中的一道重要程序.某化学兴趣小组的同学在实验室中进行了模拟实验.向含有硝酸铜和硝酸银的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣.下列说法正确的是( )
|
| A. | 滤液中最多含有三种溶质 |
|
| B. | 滤液质量比反应前原溶液质量大 |
|
| C. | 滤液中一定含有硝酸亚铁,滤渣中一定含有银 |
|
| D. | 若反应后所得滤液呈浅绿色,则滤渣中一定含有铁、铜、银 |
下列与水有关的说法正确的是( )
|
| A. | 水是一种最常见的溶剂 |
|
| B. | 自然界中的水都是纯净物 |
|
| C. | 水资源丰富不用节约用水 |
|
| D. | 过滤可以除去水中所有的杂质 |
下列物质溶于水,不能形成溶液的是( )
|
| A. | 食盐 | B. | 硝酸钾 | C. | 蔗糖 | D. | 植物油 |
下列物质的用途与性质对应不正确的是( )
| 物 质 | 用 途 | 性 质 | |
| A | 二氧化碳 | 作气体肥料 | 二氧化碳既不燃 |
| B | 熟石灰 | 改良酸性土壤 | 熟石灰能与酸发生中和反应 |
| C | 小苏打 | 治疗胃酸过多 | 小苏打能与盐酸反应 |
| D | 氮气 | 焊接金属时做保护气 | 氮气的化学性质不活泼 |
A.A B.B C.C D.D
 Si+2X↑,则X的化学式为( )
Si+2X↑,则X的化学式为( )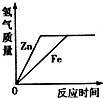

 烧也不支持燃烧
烧也不支持燃烧