题目内容
某校化学兴趣小组利用右图装置制备一氧化碳,再用一氧化碳还原三氧化二铁并检验反应产物.
查阅资料:
Ⅰ.草酸在浓硫酸存在时加热发生如下反应:H2C2O4
 CO↑+CO2↑+H2O
CO↑+CO2↑+H2OⅡ.氢氧化钠溶液可以吸收二氧化碳
Ⅲ.浓硫酸具有吸水性,可以做干燥剂
(1)实验前除了要先检查装置的气密性,还要检验______,再先点燃______(填A或D处)加热,以防止发生爆炸.
(2)其中B装置的作用______;E装置的作用______;
D装置中反应的化学方程式及现象为______ 2Fe+3CO2
【答案】分析:本题是在原有一氧化碳还原氧化铁的实验基础上增加了制取纯净的一氧化碳的实验,由题中信息,草酸分解后得到的一氧化碳中混有二氧化碳和水蒸气,因此要预先除掉二氧化碳.氢氧化钠与二氧化碳反应消耗二氧化碳,浓硫酸具有吸水性除去水分.产生的二氧化碳使澄清石灰水变浑浊,过程中可能一氧化碳过多,必须对尾气进行处理.(3)中氧化铁还原为铁,质量减轻,运用差量法可求出氧化铁的质量,再利用质量分数公式求算.
解答:解:(1)点燃或加热可燃性气体都必须验纯,利用先生成的一氧化碳排净装置内的空气.
故答案为:一氧化碳的纯度;A
(2)B装置内是氢氧化钠能吸收产生的二氧化碳,E装置则是吸收并检验二氧化碳的存在,D装置是高炉炼铁的反应;氧化铁是红色的,铁粉是黑色的.
故答案为:除去CO中混有的CO2;3检验CO还原Fe2O3是否有二氧化碳生成;CO+Fe2O3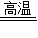 2Fe+3CO2;装置D中的粉末由红色逐渐变黑
2Fe+3CO2;装置D中的粉末由红色逐渐变黑
(3)原有样品为氧化铁(10g),反应后为剩余固体为(7.6g),减少的质量为2.4g,实质为氧元素的质量,运用差量法解题
设氧化铁的质量为X
3CO+Fe2O3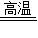 2Fe+3CO2 △m
2Fe+3CO2 △m
160 112 48
X (10-7.6)g
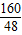 =
=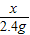
X=8g
氧化铁的质量分数为: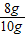 ×100%=80%
×100%=80%
故答案为:80%;称量氧化铁样品的质量10.0g
(4)一氧化碳有毒,过程中可能一氧化碳过多,必须对尾气进行处理.故答案为:没有尾气处理装置
点评:本题考查了高炉炼铁的原理、实验现象、尾气处理以及应用.要注意有毒气体不能随意排放,可燃性气体在加热或点燃前的验纯,以及净化气体的方法.
解答:解:(1)点燃或加热可燃性气体都必须验纯,利用先生成的一氧化碳排净装置内的空气.
故答案为:一氧化碳的纯度;A
(2)B装置内是氢氧化钠能吸收产生的二氧化碳,E装置则是吸收并检验二氧化碳的存在,D装置是高炉炼铁的反应;氧化铁是红色的,铁粉是黑色的.
故答案为:除去CO中混有的CO2;3检验CO还原Fe2O3是否有二氧化碳生成;CO+Fe2O3
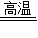 2Fe+3CO2;装置D中的粉末由红色逐渐变黑
2Fe+3CO2;装置D中的粉末由红色逐渐变黑(3)原有样品为氧化铁(10g),反应后为剩余固体为(7.6g),减少的质量为2.4g,实质为氧元素的质量,运用差量法解题
设氧化铁的质量为X
3CO+Fe2O3
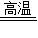 2Fe+3CO2 △m
2Fe+3CO2 △m160 112 48
X (10-7.6)g
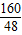 =
=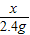
X=8g
氧化铁的质量分数为:
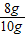 ×100%=80%
×100%=80%故答案为:80%;称量氧化铁样品的质量10.0g
(4)一氧化碳有毒,过程中可能一氧化碳过多,必须对尾气进行处理.故答案为:没有尾气处理装置
点评:本题考查了高炉炼铁的原理、实验现象、尾气处理以及应用.要注意有毒气体不能随意排放,可燃性气体在加热或点燃前的验纯,以及净化气体的方法.

练习册系列答案
相关题目
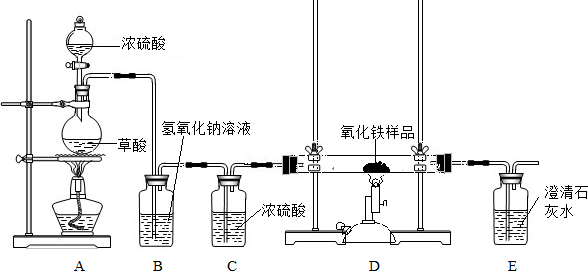
 某品牌牙膏是由多种无机物和有机物组成的,它包括摩擦剂、洗涤泡沫剂、粘合剂、保湿剂、甜味剂、芳香剂和水分.其中摩擦剂用量达45%,该物质难溶于水,是初中常见的一种化学物质.某校化学兴趣小组利用初中知识对该牙膏的酸碱性和摩擦剂成分进行了研究探讨:
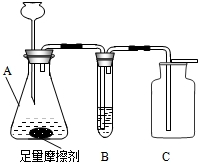
某品牌牙膏是由多种无机物和有机物组成的,它包括摩擦剂、洗涤泡沫剂、粘合剂、保湿剂、甜味剂、芳香剂和水分.其中摩擦剂用量达45%,该物质难溶于水,是初中常见的一种化学物质.某校化学兴趣小组利用初中知识对该牙膏的酸碱性和摩擦剂成分进行了研究探讨: 某校化学兴趣小组利用如图所示装置制取并收集一定体积的氧气.
某校化学兴趣小组利用如图所示装置制取并收集一定体积的氧气.