题目内容
16.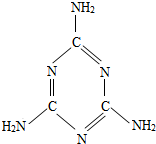 震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.
震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.(1)三聚氰胺的化学式为:C3H6N6;
(2)三聚氰胺中氮元素的质量分数为66.7%;
(3)奶粉中蛋白质含量为15~20%,蛋白质中含氮量平均为16%,若不法分子在某品牌奶粉1袋(400g)中加了1g三聚氰铵,相当于增加了4.17 g蛋白质.
分析 (1)根据三聚氰胺的分子结构图可判断分子中的原子个数,然后确定化学式;
(2)根据化学式及原子的相对原子质量来计算元素的质量分数;
(3)某个品牌奶粉中蛋白质中含氮量平均为16%,某品牌奶粉1袋(400g),结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)由三聚氰胺的分子结构图可知1个分子中含有3个碳原子、6个氢原子、6个氮原子,则化学式为C3H6N6,故答案为:C3H6N6;
(2)由三聚氰胺的化学式为C3H6N6,则三聚氰胺中氮元素的质量分数为$\frac{14×6}{12×3+1×6+14×6}×100%$=66.7%;故填:66.7%;
(3)某品牌奶粉1袋(400g)中加了1g三聚氰铵,其中含氮元素的质量为1g×66.7%=0.667g;相当于增加了蛋白质的质量为0.667g÷16%≈4.17g.
故填:4.17.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
11.以下几种二氧化碳的用途中,既利用了CO2的物理性质,又利用了它的化学性质的是( )
| A. | 人工降雨 | B. | 植物的光合作用 | C. | 制尿素、化肥 | D. | 灭火器灭火 |
8.将一小块银白色的金属钠放置在空气中会发生下列变化:钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2CO3,
猜想3:①Na2O和Na2O2
【实验探究一】
【继续探究】钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式⑥Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为⑦O2
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 ⑧不是碱性氧化物(填“是”或“不是”).
【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2CO3,
猜想3:①Na2O和Na2O2
【实验探究一】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | ②无气泡产生 | 猜想1正确 |
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量 ③CaCl2溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3 和NaOH |
| 2.过滤、取少量滤液加入④无色的酚酞试液 | ⑤变成红色 |
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式⑥Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为⑦O2
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 ⑧不是碱性氧化物(填“是”或“不是”).
5.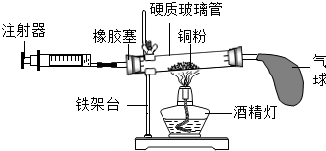 用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )
用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )
 用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )
用如图所示装置来测定空气中氧气的含量,对该实验认识错误的是( )| A. | 铜粉用量过少,实验结果会偏小 | |
| B. | 实验结束后冷却到室温才能读数 | |
| C. | 气球的作用是调节气压,使氧气完全反应 | |
| D. | 在正常操作情况下,反应结束后消耗氧气的总体积应该是反应前注射器内气体体积的$\frac{4}{5}$ |
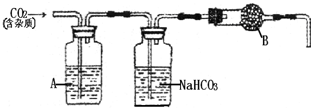
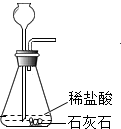
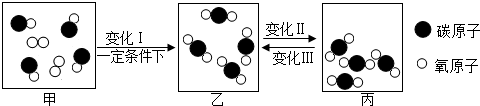
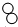 ”和“
”和“ ”的化学计量数之比为1:2.
”的化学计量数之比为1:2.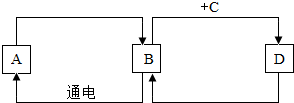 已知A、B、C、D是初中化学常见的物质.它们之间的相互转化关系如图所示,其中A被看作是理想的“绿色能源”,B在常温下是一种无色液体,C可用于灭火.(部分反应物、生成物和反应条件未标出)
已知A、B、C、D是初中化学常见的物质.它们之间的相互转化关系如图所示,其中A被看作是理想的“绿色能源”,B在常温下是一种无色液体,C可用于灭火.(部分反应物、生成物和反应条件未标出)