题目内容
(1)求碳酸钙中钙元素的质量分数.
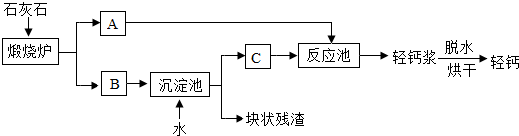
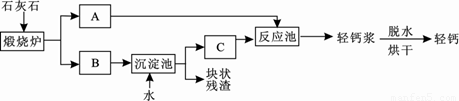
(2)工业上通过煅烧石灰石来制取二氧化碳.如果制取88千克二氧化碳,至少需要多少碳酸钙?
CaCO3
CaO+CO2↑.
(2)工业上通过煅烧石灰石来制取二氧化碳.如果制取88千克二氧化碳,至少需要多少碳酸钙?
CaCO3
| ||
分析:(1)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)根据分解的生成的二氧化碳的质量,由反应的化学方程式计算出参加反应的碳酸钙的质量即可.
| 相对原子质量×原子个数 |
| 相对分子质量 |
(2)根据分解的生成的二氧化碳的质量,由反应的化学方程式计算出参加反应的碳酸钙的质量即可.
解答:解:(1)碳酸钙中钙元素的质量分数为
×100%=40%.
(2)设需要碳酸钙质量为X
CaCO3
CaO+CO2↑
100 44
X 88Kg
=
X=200Kg
答:(1)碳酸钙中钙元素的质量分数为;(2)至少需要200Kg碳酸钙.
| 40 |
| 40+12+16×3 |
(2)设需要碳酸钙质量为X
CaCO3
| ||
100 44
X 88Kg
| 100 |
| X |
| 44 |
| 88Kg |
答:(1)碳酸钙中钙元素的质量分数为;(2)至少需要200Kg碳酸钙.
点评:本题难度不大,掌握化学式与化学方程式的有关计算并能灵活运用是正确解答本题的关键.

练习册系列答案
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
 如图为“XX补钙剂”标签上的部分标示内容.根据碳酸钙CaCO3化学式计算
如图为“XX补钙剂”标签上的部分标示内容.根据碳酸钙CaCO3化学式计算