题目内容
某课外小组在研究金属与酸的化学反应时,设计了以下三个实验.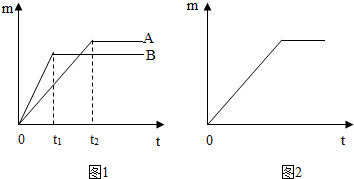
(1)不同金属与酸反应的速率不同.
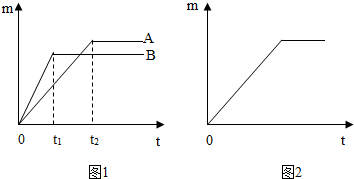
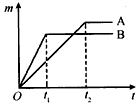
取质量相等的铁片和锌片,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示.
①锌比铁的金属活动性______.(填“强”或“弱”)
②B表示的金属是______,请写出金属B与稀盐酸反应的化学方程式______.
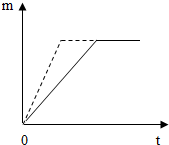
(2)金属与不同质量分数的盐酸反应的快慢不同.取质量相等的锌片,分别放入5%、20%的足量稀盐酸中.实验表明盐酸浓度越大,反应速率越快.5%的盐酸与锌片反应生成氢气的质量(m)与反应时间(t)的关系曲线如图2所示.请在该图上用虚线“…”补画出20%的盐酸与锌片反应m与t的关系曲线.
(3)温度对金属与盐酸反应速率也有影响.实验表明,温度越高,盐酸与金属反应的速率越快.请你设计一个实验方案证明这一结论.你的方案是______.
 解:(1)①依据金属活动性顺序表可知锌的活动性比铁强;
解:(1)①依据金属活动性顺序表可知锌的活动性比铁强;②因为同价态金属与酸反应时生成的氢气量与其相对原子质量呈反比,所以取质量相等的铁片和锌片,分别放入溶质质量分数相同的足量稀盐酸中时锌生成的氢气量小,所以B是锌,与盐酸反应的方程式为:Zn+2HCl=ZnCl2+H2↑;
(2)由于盐酸浓度越大,反应速率越快,所以放入到20%的盐酸中时锌与盐酸反应的速度要比放入到5%的盐酸中快,所以反应完全的时间要短,但氢气量没有变化.
(3)要想证明温度对金属与盐酸反应速率也有影响,就需要对实验中除温度以外的其它条件进行控制,创设相同的条件(温度不同),可进行如下设计:取两个烧杯,分别加入等质量的同种金属,再分别加入质量相等的足量的溶质质量分数相同的稀盐酸,对其中一个烧杯加热.可以观察到温度越高,气泡生成的越快,即盐酸与金属反应的速率越快,.
故答案为:(1)①强;②锌或Zn; Zn+2HCl=ZnCl2+H2↑;
(2)如图;
(3)取两个烧杯,分别加入等质量的同种金属,再分别加入质量相等的足量的溶质质量分数相同的稀盐酸,对其中一个烧杯加热.可以观察到温度越高,盐酸与金属反应的速率越快.
分析:(1)①依据金属活动性顺序的情况分析;
②依据同价态金属与酸反应时生成的氢气量与其相对原子质量呈反比分析判断;
(2)依据题干中关于盐酸浓度越大,反应速率越快的原理对金属与酸反应时的图象进行绘制即可;
(3)要想证明温度对金属与盐酸反应速率也有影响就需要对实验中除温度以外的其它条件进行控制,创设相同的条件(温度不同),只有这样才能合理的得出结论.
点评:此题是一道实验探究题,主要是考查了金属与酸的反应,只要掌握了金属与酸的反应规律以及控制变量法进行实验,便能顺利解题.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
某课外小组对一些金属单质和化合物的性质进行研究,下表是铝与氯化铜溶液反应实验报告的一部分:
| 实验报告 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的氯 化铜溶液中. | 产生气泡,析出疏松的红色固体,溶液逐渐 变为无色. |
| 反应结束后过滤. | |
| 红色固体用蒸馏水洗涤后,置于潮湿的空气中. | 一段时间后固体由红色变为绿色(视其成分为铜绿). |
| 将绿色固体加热. | 最后只得到黑色固体. |
(2)若测得氯化铜溶液的pH小于7,则导致溶液呈现酸性的离子是________(在“Cu2+”或“Cl-”中选择),请设计简单的方案进行验证________;
(3)写出实验中红色固体变为绿色的有关化学方程式:________.