题目内容
下列五种溶液:①NaOH溶液、②Ba(OH)2溶液、③Na2SO4溶液、④稀硝酸、⑤混有少量硝酸的MgSO4溶液.(1)指出其中属于碱溶液的是______(选填序号);
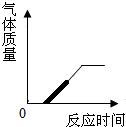
(2)若将Ba(OH)2溶液逐滴加入到混有少量硝酸的MgSO4溶液中,所得沉淀的质量与加入的Ba(OH)2的质量变化符合下列图象的是______(选填序号).

【答案】分析:(1)根据碱的构成可知,碱是由金属阳离子和氢氧根离子构成的来解答;
(2)很据反应的先后顺序可知,有少量硝酸的MgSO4溶液中加入Ba(OH)2后,Ba2+与溶液中的SO42-反应生成既不溶于水又不溶于酸的BaSO4沉淀,OH-先跟硝酸中的H+发生中和反应,待H+完全反应,OH-与Mg2+开始生成Mg(OH)2沉淀来分析解答.
解答:解:(1)因NaOH是由钠离子和氢氧根离子构成,Ba(OH)2是由钡离子和氢氧根离子构成,其它物质构成中不符合碱的概念,则①②是碱溶液,故答案为:①②;
(2)因含少量硝酸的MgSO4溶液中加入Ba(OH)2后,Ba2+与溶液中的SO42-反应生成既不溶于水又不溶于酸的BaSO4沉淀,OH-先跟硝酸中的H+发生中和反应.待H+完全反应,OH-与Mg2+开始生成Mg(OH)2沉淀,即第一段沉淀是BaSO4,生成BaSO4的同时OH-和H+完全反应,产生水;(第一阶段,在硫酸根离子减少的同时,镁离子没有减少,此时由于是酸性环境,所以不能生成氢氧化镁沉淀).第二段斜率很大,是因为氢离子完全反应后,溶液中仍含有SO42-,同时还有 Ba(OH)2同时和MgSO4反应生成沉淀BaSO4和Mg(OH)2,所以沉淀多;(第二阶段由于加入的氢氧化钡和硫酸镁是正好成比例反应,导致第一阶段相对剩余的镁离子还是依旧剩余).第三段斜率又变小,溶液中SO42-反应完全,只有显得偏多的Mg2+与OH-生成Mg(OH)2沉淀,
直至曲线平直Ba(OH)2过量不再产生沉淀,故答案为:C.
点评:本题难度较大,考查化学反应与图象的对应关系,明确反应的先后顺序及每段对应的化学反应时解答的关键,还应关注曲线的起点、折点及趋势的特殊意义及不同段曲线的斜率来解答.
(2)很据反应的先后顺序可知,有少量硝酸的MgSO4溶液中加入Ba(OH)2后,Ba2+与溶液中的SO42-反应生成既不溶于水又不溶于酸的BaSO4沉淀,OH-先跟硝酸中的H+发生中和反应,待H+完全反应,OH-与Mg2+开始生成Mg(OH)2沉淀来分析解答.
解答:解:(1)因NaOH是由钠离子和氢氧根离子构成,Ba(OH)2是由钡离子和氢氧根离子构成,其它物质构成中不符合碱的概念,则①②是碱溶液,故答案为:①②;
(2)因含少量硝酸的MgSO4溶液中加入Ba(OH)2后,Ba2+与溶液中的SO42-反应生成既不溶于水又不溶于酸的BaSO4沉淀,OH-先跟硝酸中的H+发生中和反应.待H+完全反应,OH-与Mg2+开始生成Mg(OH)2沉淀,即第一段沉淀是BaSO4,生成BaSO4的同时OH-和H+完全反应,产生水;(第一阶段,在硫酸根离子减少的同时,镁离子没有减少,此时由于是酸性环境,所以不能生成氢氧化镁沉淀).第二段斜率很大,是因为氢离子完全反应后,溶液中仍含有SO42-,同时还有 Ba(OH)2同时和MgSO4反应生成沉淀BaSO4和Mg(OH)2,所以沉淀多;(第二阶段由于加入的氢氧化钡和硫酸镁是正好成比例反应,导致第一阶段相对剩余的镁离子还是依旧剩余).第三段斜率又变小,溶液中SO42-反应完全,只有显得偏多的Mg2+与OH-生成Mg(OH)2沉淀,
直至曲线平直Ba(OH)2过量不再产生沉淀,故答案为:C.
点评:本题难度较大,考查化学反应与图象的对应关系,明确反应的先后顺序及每段对应的化学反应时解答的关键,还应关注曲线的起点、折点及趋势的特殊意义及不同段曲线的斜率来解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 26、了解物质构成的微观奥秘,能帮助我们更好地认识物质变化的本质.
26、了解物质构成的微观奥秘,能帮助我们更好地认识物质变化的本质.
 分别表示N2、H2、NH3三种分子.为了便于理解,我们将在固体催化剂表面(用
分别表示N2、H2、NH3三种分子.为了便于理解,我们将在固体催化剂表面(用 表示)合成氨的过程简化为下图中的五个步骤,请按照正确的步骤进行排序
表示)合成氨的过程简化为下图中的五个步骤,请按照正确的步骤进行排序

 (2013?密云县一模)A、B、C、D、E都是初中化学常见的物质,分别由H、C、O、Cl、Na、Ca等六种元素中的两种或几种组成,根据下列信息回答问题.
(2013?密云县一模)A、B、C、D、E都是初中化学常见的物质,分别由H、C、O、Cl、Na、Ca等六种元素中的两种或几种组成,根据下列信息回答问题.