题目内容
下表是KCl在不同温度时的溶解度.
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度/g |
27.6 |
31.0 |
34.0 |
37.0 |
x |
42.6 |
45.5 |
小明为测定x的值,取4份40℃的水各50g,分别进行实验,并记录数据如下表.
|
实验编号 |
实验1 |
实验2 |
实验3 |
实验4 |
|
KCl质量/g |
5 |
15 |
25 |
35 |
|
溶液质量/g |
55 |
65 |
70 |
70 |
请回答下列问题.
(1)实验中需要用到的仪器有 (只写一种).
(2)要使实验2的溶液达到饱和,可采取的方法是 .
(3)由实验可知,40℃时KCl的溶解度x为 g.
(4)小明现要配制质量分数为30%的KCl溶液100g,为达实验目的其主要操作是 .
(1)烧杯 (2)增加溶质、降低温度、蒸发溶剂 (3)40
(4)水的温度升高至50℃以上,称取30gKCl固体溶于70g水中.
【解析】
试题分析:(1)进行溶解实验时需要的玻璃仪器有烧杯、玻璃棒等,故填:烧杯;
(2)根据表1可知氯化钾的溶解度随温度升高而增大,故要使其不饱和溶液变为饱和溶液,可以采用增加溶质、降低温度或是蒸发溶剂的方法,故填:增加溶质、降低温度、蒸发溶剂;
(3)根据表2提供的数据,所取水的质量为50g,当加入氯化钾25g和35g时,溶液的质量都是70g,说明40℃时50g水中最多溶解氯化钾20g,即100g水中最多溶解40g故填:40;
(4)配制质量分数为30%的KCl溶液100g,则需要氯化钾的质量为100g×30%=30g,需要水的质量为100g﹣30g=70g,此时100g水中溶解氯化钾的质量为: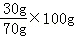
≈42.9g,根据表1溶解度,可知温度需要升高到50℃以上,故填:水的温度升高至50℃以上,称取30gKCl固体溶于70g水中.
考点:固体溶解度的影响因素;一定溶质质量分数的溶液的配制;饱和溶液和不饱和溶液相互转变的方法;固体溶解度的概念.
点评:本题考查了固体物质溶解度的有关计算,完成此题,可以依据提供的信息进行.

 名校课堂系列答案
名校课堂系列答案 KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
(2)将饱和的硝酸钾溶液变成同温下的不饱和溶液,可采用的方法是________.
(3)由表中数据分析可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是________.
(4)硝酸钾与少量的氯化钾混合,得到较纯净的硝酸钾的操作是________.
(5)要配制50g溶质质量分数为5%的KCl溶液,需要的实验仪器有天平(含砝码)、烧杯、药匙、量筒、________.
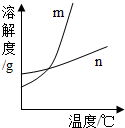 KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题: