题目内容
高铁酸钠(Na2FeO4)是一种新型高效的水处理剂.下列有关高铁酸钠的说法正确的是( )
A.属于氧化物
B.钠、铁、氧三种元素质量比是2:1:4
C.铁元素化合价为+6
D.由两种金属和一种非金属组成
【考点】化学式的书写及意义;从组成上识别氧化物;有关元素化合价的计算;元素质量比的计算.
【专题】化学用语和质量守恒定律.
【分析】利用氧化物由两种元素组成,化学式表示的意义及化合物中各元素化合价代数和为零解决此题.
【解答】解:A、氧化物由两种元素组成而高铁酸钠由三种元素组成,故A错误;
B、高铁酸钠中钠、铁、氧三种元素的质量比为(23×2):56:(16×4)=23:28:32,故B错误;
C、化合物中各元素化合价代数和为零,钠显+1价,氧显﹣2价,因此高铁酸钠中铁元素的化合价为+6价,故C正确;
D、高铁酸钠由两种金属元素和一种非金属元素组成,故D错误.
故选:C.
【点评】此题是对化学式的意义及简单计算的考查,属基础性训练题是对化学式相关问题的强化与巩固.

 阅读快车系列答案
阅读快车系列答案甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如图所示的四组实验方案.
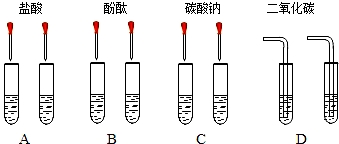
(1)其中能达到实验目的是
(2)在C组实验中发生的化学方程式为
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有 物质生成(填化学式),滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和 三种物质中的一种,或是三种物质两两混合组成的混合物.
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证.请根据要求完成下列空白:
| 实验内容 | 预测现象 | 结论 |
| 取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
| ②若无沉淀生成,溶液呈红色 | 物质是氢氧化钙 | |
| ③若有白色沉淀,溶液呈红色 |
|
(6)乙同学认为甲同学第②步验证的结论不严密,原因是 .
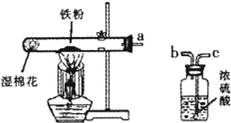
“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究.
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关.
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验.
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 30% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 20% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式 .
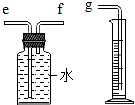
(2)小兵用如图装置收集并测量氢气的体积,其中量筒的作用是 ,
氢气应从 (填e或f或g)管通入.
(3)若用该收集CO2,并测量生成的CO2气体的体积,其中在水面上放一层植物油目的是 ;
【收集证据】(4)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 .
【得出结论】(5)结论是
【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分)
(6)下表是小兵第①组实验的详细数据.
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的快慢的变化并解释原因 .
(7)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证. .