题目内容
14.实验装置如图1所示:
(1)某同学用氯酸钾和二氧化锰共热制备和收集氧气,他应选用的气体发生装置是A(填序号)来制取.用装置E来收集,其原因是氧气不易溶于水.
(2)用氯酸钾和二氧化锰共热制备氧气的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,它属于分解反应(写出基本反应类型).此反应中氯酸钾、氯化钾、氧气的质量比是:245:149:96.
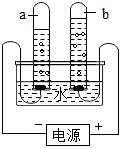
(3)如图2是通电分解水的实验装置.在实验过程中,试管a中产生的气体是氧气.A端是电源的负极.
分析 (1)根据制取气体的反应物的状态及反应条件确定发生装置,根据气体的性质确定收集装置;
(2)根据用氯酸钾和二氧化锰共热制备氧气的化学方程式分析回答;
(3)根据电解水实验的原理和结论分析回答.
解答 解:(1)某同学用氯酸钾和二氧化锰共热制备和收集氧气,属于加热固体制取气体,试管口应稍向下倾斜,他应选用的气体发生装置是A来制取.用装置E来收集,其原因是氧气不易溶于水.
(2)用氯酸钾和二氧化锰共热制备氧气的化学方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该反应符合“一变多”的特征,属于分解反应,此反应中氯酸钾、氯化钾、氧气的质量比是:245:149:96.
(3)由通电分解水的实验装置可知,在实验过程中,试管a中产生的气体是较少是氧气.试管b中产生的气体是较多是氢气,所连接的A端是电源的负极.
故答为:(1)A,氧气不易溶于水;(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,分解,245:149:96;(3)氧气,负.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式书写和注意事项等,气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
5. 2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.据图判断,有关铱的说法不正确的是( )
2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.据图判断,有关铱的说法不正确的是( )
 2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.据图判断,有关铱的说法不正确的是( )
2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.据图判断,有关铱的说法不正确的是( )| A. | 铱元素是非金属元素 | B. | 铱的元素符号是Ir | ||
| C. | 铱原子的原子序数为77 | D. | 铱元素的相对原子质量为192.2 |
2.“墙角数枝梅,凌寒独自开,遥知不是雪,为有暗香来”(王安石《梅花》).诗人在远处就能闻到梅花香味的原因是 ( )
| A. | 分子是可分的 | B. | 分子之间有间隔 | ||
| C. | 分子在不断地运动 | D. | 分子很小 |
9.实验室制取CO2并回收CaCl2,下列操作不规范的是( )
| A. |  用如图装置检查气密性 | |
| B. |  用如图装置乙收集CO2 | |
| C. |  用如图装置分离固体杂质和CaCl2溶液 | |
| D. |  用如图装置蒸干溶液得CaCl2晶体 |
19.下列物质对空气不会造成污染的是( )
| A. | 二氧化氮 | B. | 二氧化硫 | C. | 氮气 | D. | 沙尘暴 |
4.如图所示的实验中,发生了化学变化的是( )
| A. |  干冰升华 | B. |  CO2与水混合 | ||
| C. |  CO2密度研究 | D. |  水的净化 |
 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: