题目内容
二甲醚燃料具有高效率和低污染的优点。现在我国部分城市已开始使用二甲醚作为公交车的燃料。二甲醚燃烧的化学方程式为
CaHbOd(二甲醚 )+3O2
)+3O2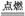 2CO2+3H2O
2CO2+3H2O
请通过计算回答:
(1)a= ;b= ;d= 。
(2)23 g二甲醚充分燃烧需要多少克氧气?生成多少克二氧化碳?
【解析】根据化学反应前后各原子的种类与数目不变,可以确定a=2,b=6,c=1;根据二甲醚燃烧的化学方程式找出二甲醚与氧气及二氧化碳的质量关系,由二甲醚的质量可以分别计算燃烧需要氧气的质量及生成的二氧化碳的质量。
答案:(1)2 6 1
(2)解:设23 g二甲醚充分燃烧需要氧气的质量为x,生成二氧化碳的质量为y。
C2H6O(二甲醚)+3O2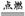 2CO2+3H2O
2CO2+3H2O
4 6 96 88
6 96 88
23 g x y
46∶96=23 g∶x x=48 g
46∶88=23 g∶y y=44 g
答:需要氧气的质量为48 g,生成二氧化碳的 质量为44 g。
质量为44 g。

在一个密闭容器中加入4种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 2 | 2 | 21 | 5 |
| 反应后质量/g | 10 | 2 | 9 | 待测 |
通过分析,判断下列说法不正确的是 ( )
A.甲是生成物
B.测得反应后丁的质量为4 g
C.乙可能是催化剂
D.该反应是分解反应
在一个密闭的钢筒内有甲、乙、丙、丁四种物质,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量/g | 64 | 10 | 1 | 25 |
| 反应后质量/g | 54 | 37 | 9 |
已知甲的相对分子质量为丁的2倍,则该反应的化学 方程式中甲与丁的化学计量数之比为( )
方程式中甲与丁的化学计量数之比为( )
A.1∶2 B.1∶1
C.2∶1 D.2∶3
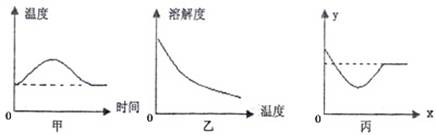
 2C+2D的反应中,14 g A完全反应生成44 g C和18 g D,若A的相对分子质量为28,则B的相对分子质量是 ( )
2C+2D的反应中,14 g A完全反应生成44 g C和18 g D,若A的相对分子质量为28,则B的相对分子质量是 ( )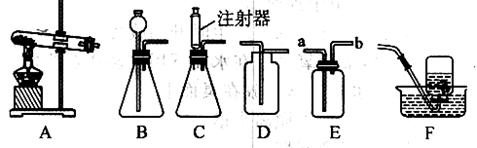
 理是
理是